Симптомы и лечение дистрофии печени: зернистой, белковой, токсической, гидропической, жировой
Содержание:
- Очаговая дистрофия печени
- Липидозы
- Симптоматика заболевания
- Диагностика заболевания
- Симптомы дистрофии печени
- Симптомы
- Из Википедии — свободной энциклопедии
- Что такое дистрофии роговицы?
- Диагностика
- Диффузная дистрофия печени
- Строение, структура и функции
- Диагностика заболевания
- Паренхиматозная дистрофия печени
- Острая печёночная дистрофия
- Классификация
- Белковая ДП
- НАРУШЕНИЯ ОБМЕНА НУКЛЕОПРОТЕИНОВ
- Внеклеточные диспротеинозы
- Классификация
- УГЛЕВОДНЫЕ СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
- СМЕШАННЫЕ ДИСТРОФИИ
- Острая дистрофия печени
- Диффузная дистрофия
- Диета при дистрофии печени
Очаговая дистрофия печени
Очаговая дистрофия печени представляет определенные сложности в диагностировании данного заболевания в силу того что хотя имеет место ухудшение функционирования печени зафиксировать эти патологические изменения посредством лабораторных исследований представляется крайне затруднительным.
Исходя из тех причин, которыми вызвана очаговая печеночная дистрофия, в каждом отдельном случае характерным является наличие различных объективных и субъективных симптомов и проявлений этой болезни у каждого конкретного пациента.
Очаговая дистрофия печени, возникающая в частности как следствие регулярной интоксикации большими дозами алкоголя, проявляется в таких явлениях как появление отдышки, ухудшение аппетита и т. д. в некоторых случаях пациенты отмечают возникновение неприятных ощущений и тяжести в области правого подреберья. Такие симптомы характеризуются увеличением их интенсивности во время движения.
Зачастую выявление жировой инфильтрации печени становится возможным только при проведении магнитно-резонансной – МРТ и компьютерной томографии. Данные диагностические методики представляют собой наиболее эффективный способ обнаружения у пациента очаговой дистрофии печени.
[], [], [], [], [], []
Липидозы
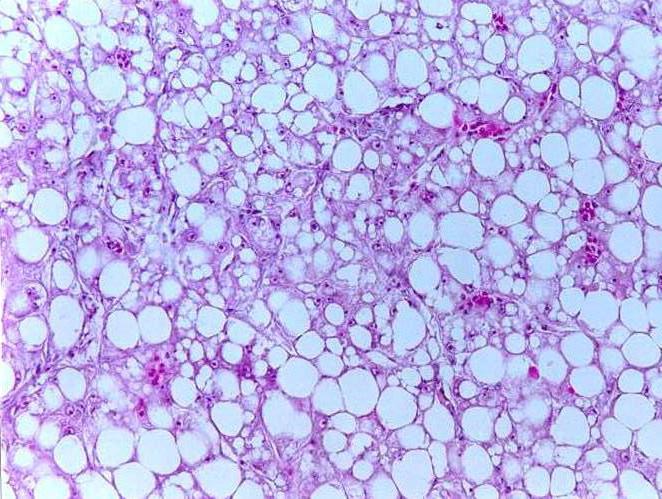
Липиды содержатся в каждой клетке, они могут находиться как отдельно, так и в комплексе с белками и быть структурными единицами мембраны клеток, а также других ультраструктур. Кроме того, в цитоплазме находится глицерин и жирные кислоты. Для того чтобы обнаружить их в тканях используются специальные методы фиксирования и окрашивания, например суданом черным или красным, осмиевой кислотой, сульфатом нильского голубого. После специфической подготовки препараты тщательно осматривают в электронный микроскоп.
Паренхиматозная жировая дистрофия проявляется в виде чрезмерного накопления жиров там, где они должны быть, и появления липидов там, где их быть не должно. Как правило, накапливаются нейтральные жиры. Органы мишени те же, что и при белковой дистрофии – сердце, почки и печень.
Жирова паренхиматозная дистрофия миокарда начинается с появления в миоцитах очень мелких капелек жира, т. н. пылевидное ожирение. Если процесс не останавливается на этом этапе, то со временем капли сливаются и становятся больше, пока не займут всю цитоплазму. Органеллы при этом распадаются, исчерченность мышечных волокон пропадает. Заболевание локально проявляется около венозного сосудистого русла.
Макроскопически паренхиматозная жировая дистрофия проявляется по-разному, все зависит от стадии процесса. В самом начале диагноз можно поставить только под микроскопом, но со временем сердце увеличивается за счет растягивания камер, стенки его становятся тонкими и дряблыми, при разрезе миокарда видны грязно-желтые полосы. Патофизиологи придумали название этому органу: «тигровое сердце».
Жировая дистрофия паренхиматозных органов развивается по трем основным механизмам.
- Повышенное поступление свободных жирных кислот в клетки миокарда.
- Нарушение жирового обмена.
- Распад липопротеидных структур внутри клетки.
Чаще всего эти механизмы запускаются во время гипоксии, инфекции (дифтерия, туберкулез, сепсис) и интоксикации организма хлором, фосфором или мышьяком.
Как правило, жировая дистрофия обратима, а нарушения клеточных структур восстанавливаются со временем. Но если процесс сильно запущен, то все заканчивается гибелью ткани и органа. Клиницисты различают следующие заболевания, связанные с накоплением жиров в клетках:
— болезнь Гоше;
— болезнь Тея-Сакса;
— болезнь Ниманна-Пика и другие.
Симптоматика заболевания

Чаще всего патологию диагностируют у пациентов в возрасте от десяти до сорока лет. Ткани органа зрения у каждого человека имеют специфические характеристики, но выделяют несколько признаков патологии, характерных для всех больных:
- Слизистая оболочка приобретает красноватый оттенок;
- Усиленное слезотечение;
- Непереносимость яркого света;
- Болевые ощущения;
- Чувство присутствия постороннего предмета в глазах;
- Падение остроты зрения;
- Резь.
| Если патология прогрессирует, то роговая оболочка отекает и мутнеет, что отрицательно сказывается на здоровье зрительного аппарата. |
Диагностика заболевания
Диагностика ДП является затруднительной, так как традиционные лабораторные исследования оказываются неэффективными, несмотря на расстройства функциональности железы.
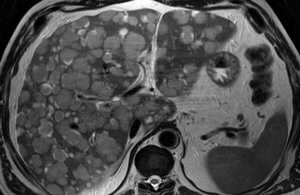
КТ и МРТ – это основные методы выявления дистрофии печени
Заболевание, как правило, протекает бессимптомно, единственный признак патологии – это гепатомегалия. Эхогенность печени при УЗИ остаётся в пределах нормы, а иногда даже повышается, поэтому отличить ДП от цирроза или фиброза достаточно тяжело. Ультразвуковое исследование позволяет выявить зоны с повышенной эхогенностью. Участки с низкой эхогенностью можно определить с помощью КТ. Компьютерная и магнитно-резонансная томография – это наиболее информативные методы распознавания ДП. С их помощью можно определить очаговый гепатоз печени.
Для выявления патологии проводят биопсию. При патоморфологическом исследовании тканей врач определит избыточное скопление жиров.
Симптомы дистрофии печени
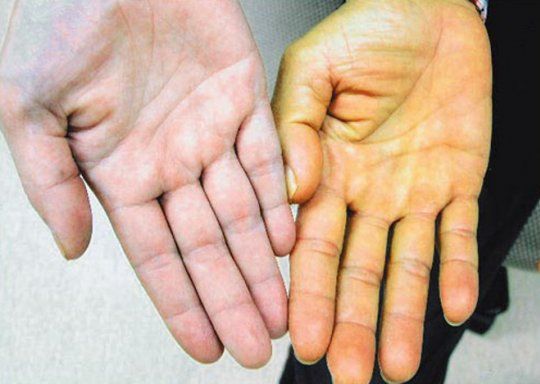
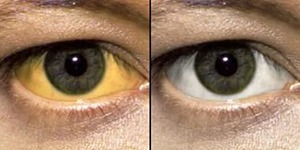
Симптомы дистрофии печени в большинстве случаев являются выраженными в крайне слабой степени. Жалобы пациентов с данным заболеванием по поводу каких-либо связанных с его наличием тревожащих явлений, как правило, ими не изъявляются. Развитие патологического процесса отличается медленно протекающим прогрессом и не явностью клинических проявлений. Однако по мере того как болезнь прогрессирует, могут возникать тупые болевые ощущения в области правого подреберья, возможно появление тошноты, рвоты, нарушается стул. В незначительном количеств случаев дистрофия печени может проявляться сильными болями в животе, уменьшением массы тела, зудом и желтушностью кожных покровов.
Симптомы дистрофии печени при токсическом типе заболевания и с массивными некрозами характеризуются возникновением гиперплазии расположенных рядом с портальной веной лимфатических узлов и селезенки. Проявлениями дистрофии печени также являются множественные кровоизлияния, которые могут появляться в коже, в слизистых и в серозных оболочках. Имеют место некротические явления и изменения дистрофического характера, происходящие в тканях, и затрагивающих также миокард сердца, поджелудочную железу.
Симптомы
Симптомы дистрофии печени чаще всего слабо выражены, и больной может просто не обратить на них внимание. Как правило, пациенты не жалуются на какие-либо тревожащие явления
Патологический процесс развивается медленно, а клиническая картина не явная.

По мере развития ДП возникает тупая боль справа под рёбрами, тошнота, гепатомегалия и т.д.
Однако со временем проявляются следующие признаки:
- тупая боль справа под рёбрами;
- гепатомегалия;
- тошнота;
- извержение рвотных масс;
- расстройства стула.
В редких случаях дистрофические изменения железы сопровождаются сильной болью в животе, резким снижением веса, зудом, окрашиванием кожи и слизистых оболочек в желтый оттенок.
Обычно симптомы ДП разделяют по типу патологии. При токсической дистрофии печени с распространённым некрозом (отмирание тканей) паренхимы органа наблюдается усиленный рост гепатоцитов, которые находятся рядом с воротной веной лимфоузлов и селезёнки. Проявляется ДП множественными кровотечениями в кожных покровах, внутренних и серозных оболочках. Кроме того, наблюдаются некротические и дистрофические изменения в тканях, которые затрагивают сердечную мышцу и поджелудочную железу.
Токсическая ДП с хроническим течением со временем прогрессирует в крупноузловой цирроз (тот, который развивается вследствие распространённого некроза паренхимы органа). При отсутствии лечения повышается вероятность смерти пациента вследствие дисфункции печени или гепаторенального синдрома (тяжёлая функциональная острая почечная недостаточность).
Из Википедии — свободной энциклопедии
Белковая дистрофия (диспротеинозы) — заболевания, связанные с нарушением обмена белка. Относится к одной из трех видов дистрофий (к паренхиматозной дистрофии).
Белок является одним из основных компонентов клеток и тканей. Его масса составляет примерно 45 % от массы сухого остатка тела. Белок в организме не депонируется, и поэтому при дефиците мобилизируются белки мышц, кожи, внутренних органов. Интегральным показателем общего уровня белкового обмена является азотистый баланс, то есть суточная разница между азотом, поступающие в организм с пищей, и количеством его, выделяемым с мочой и калом.(существуют три вида азотистого баланса: нулевой, положительный, отрицательный).
Основные проявления дефицита белка:
- снижение веса
- гипопротеинемия(понижение содержания белка в крови)
- отёки
- отрицательный азотистый баланс(на 15-25 % ниже нормы)
- иммунодефицитное состояние в результате нарушения образования лимфоцитов
- задержка физического и умственного развития
При избытке белка в организме:
- положительный азотистый баланс
- гиперпротеинемия
- диспепсические расстройства
Различают приобретённые и врождённые белковые дистрофии.
К приобретённым относятся:
- зернистая дистрофия — ранняя стадия дистрофии обычно в клетках, сердце, почках. Происходит набухание внутриклеточной структуры, высвобождается белок и уплотняется, становится похож на мелкие зёрна, а цитоплазма становится мутной. При устранении патологического фактора происходит восстановление клеток. Однако если патологический фактор не устранен переход в гиалиново-капельную, гидропическую, жировую дистрофии
- гиалиново-капельная дистрофия — более глубокое повреждение клеток. Белок уплотняется и приобретает форму светлых капель, напоминающих гиалиновый хрящ, чаще в почках или при хронической алкогольной интоксикации или хроническом застое желчи
- гидропическая дистрофия — водяночная, вакуольная. При вирусных гепатитах и оспе. Возможен некроз при гибели ядра клетки из-за вытеснения объединённой набухшей вакуоли.Исходом является фокальный или тотальный колликвационный некроз
- роговая дистрофия — избыточное образование рогового вещества в многослойном плоском эпителии.
К врождённым паренхиматозным дистрофиям относят:
- синдром мальабсорбции (недостаточное всасывание аминокислот в кишечнике),
- наследственная цистинурия — нарушение реабсорбции цистина в канальцах почек,
- фенилкетонурия
Что такое дистрофии роговицы?
Дистрофии роговицы представляют собой группу генетических, часто прогрессирующих, нарушений зрения, при которых в прозрачном внешнем слое глаза (роговице) накапливаются инородные материалы. У некоторых людей дистрофия роговицы может не вызывать симптомов; у других может вызвать значительное нарушение зрения.
Возраст начала и специфические симптомы среди различных форм дистрофии варьируют. Различные формы расстройства имеют некоторые схожие симптомы и признаки — большинство форм дистрофии роговицы поражают оба глаза (двусторонние), прогрессируют медленно, не затрагивают другие области тела и имеют тенденцию к появлению в семьях. Большинство форм наследуются как аутосомно-доминантные признаки; некоторые наследуются как аутосомно-рецессивные признаки.
Была разработана международная классификация расстройств, которая учитывает хромосомные локусы различных дистрофий роговицы, а также ответственные гены и их мутации. Традиционно эти расстройства классифицируют на основании их клинических признаков и конкретного пораженного слоя роговицы. Достижения в области молекулярной генетики (например, идентификация определенных генов заболевания) позволили лучше понять эти нарушения.
Диагностика
Исследование проходит в несколько этапов.
- Сбор анамнеза. Это данные, полученные со слов больного или его близких родственников. На их основе врач может предположить диагноз и назначить дальнейшее обследование.
- Общий осмотр. Если болезнь не прогрессирует и находится на начальном этапе, клиническая симптоматика отсутствует. Больной может жаловаться на слабость, усталость. При пальпации может прощупываться незначительно увеличенная печеночная ткань. Если болезнь запущена, врач сразу определяет желтизну кожных покровов и склер.
- Сдача лабораторных тестирований. К ним относится общий анализ крови и мочи, биохимия крови, копрограмма. Выявляется повышение лейкоцитов и СОЭ, что свидетельствует о воспалительном процессе. В биохимическом анализе будут повышены АСТ и АЛТ, которые являются печеночными ферментами, образующимися при патологии органа. Врач-лаборант определит изменение физических данных и мочи, и кала.
- УЗИ. На аппарате будет выявлено воспаление органа, его увеличение. Врач определит накопление в паренхиме посторонних веществ. Будет видно наличие диффузной и зернистой дистрофии печени.
- Биопсия и гистологический анализ. Небольшой кусочек поврежденного органа обследуют под микроскопом. Лаборант выявляет наличие посторонних веществ в виде жира, белковых образований, вакуольной жидкости. Если болезнь запущена, лаборант определит наличие большого количества соединительнотканных волокон. При переходе цирроза в рак под микроскопом будет видно озлокачествление клеток.
- МРТ, КТ. Данные от этих исследований наиболее достоверны. На экране видно увеличение органа, формирование соединительнотканных волокон, очаги воспаления измененных тканей, нарушения в воротной вене.
На основе всех полученных данных терапевт может с точностью поставить диагноз. После его подтверждения начинает экстренное лечение, чтобы не возникло осложнений.
Диффузная дистрофия печени
Диффузная дистрофия печени представляет собой патологический процесс, развивающийся в паренхиме являющейся основной тканью из которой образован этот орган. В специфических печеночных клетках гепатоцитах происходят процессы, направленные на детоксикацию поступающих в организм ядовитых веществ. Гепатоциты принимают участие в процессах пищеварения, роль их при этом сводится к секреции желчи, в которой присутствует ряд ферментов, расщепляющих жиры в желудочно-кишечном тракте. Клетки печени обеспечивают нейтрализацию вредных веществ путем их трансформации в такие, что не представляют угрозы для нормального функционирования организма, и которые впоследствии выводятся вместе с желчью.
Диффузная дистрофия печени возникает в результате того, что печёночные клетки не всегда способны переработать яд, поступающий в организм. Случается, что они не могут справиться с масштабами интоксикации, и в итоге отравление приводит к их гибели. С течением времени уничтоженные таким образом клетки замещаются фиброзной соединительной тканью. Чем более значительна степень такого поражения печени, тем больше это соответственно негативно сказывается на ее способности выполнять свои функции.
Как правило, развитию диффузного патологического прогресса в печени сопутствует аналогичный процесс затрагивающий также и поджелудочную железу, поскольку функции тих двух органов пребывают в тесной связи между собой.
[], [], [], [], [], [], [], []
Строение, структура и функции
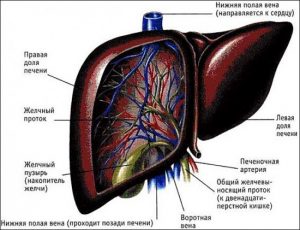 Печень имеет анатомически сложное строение.
Печень имеет анатомически сложное строение.
За ребрами, в правой верхней части туловища находится печень. При ее поражении она может смещаться или увеличиваться. Паренхима органа позволяет снабжать его кровью и выводить токсичные соединения с желчью через желчные протоки. При диффузных нарушениях тканевых покровов он не может нормально функционировать, что опасно для человека возникновением интоксикации. Эта железа внутренней секреции отвечает за очищение крови, белковый, жировой и углеводный обмены.
Структура паренхимы печени однородная, она представляет собой призматичной формы доли, входящие одна в другую (гепатоциты). Их количество достигает миллиона, а каждая долька имеет диаметр до 2 мм. Между ними находятся желчевыводящие пути, кровеносные сосуды и особое соединительное вещество. Такое строение позволяет осуществлять органу такие функции, как:
- Детоксикация. Паренхиматозная структура нейтрализует токсичные вещества, всасываемые кишечником, такие как лекарственные препараты, кофеин, алкоголь, консерванты и яды животного и растительного происхождения.
- Метаболизм. Налаживает биохимический метаболизм белков, жиров, углеводов, витаминов и микроэлементов. Регулирует уровень гликопротеинов, холестерина и гликогена в крови.
- Секреторная функция. Способствует выделению и транспортировке желчи по желчным протокам.
- Накопление. Сохраняет полезные продукты обмена веществ, такие как витамины групп A, B, D, C и F. С кровотоком они попадают в систему организма, помогая его жизнедеятельности.
Диагностика заболевания
Одним визуальным осмотром поставить диагноз практически нереально. Дистрофия сопровождается симптоматикой, которая характерна для многих глазных заболеваний. Поэтому доктор назначает ряд дополнительных процедур.
Прежде всего, пациента отправляют на биомикроскопию. Суть методики заключается в бесконтактном способе осмотра органа зрения с помощью щелевой лампы. Устройство по внешнему виду напоминает микроскоп, оснащенный собственным источником света.
С помощью лампы окулист получает возможность детально рассмотреть все элементы передней части ока, используя достаточно большое увеличение. Биомикроскопия позволяет не только обнаружить аномалию, но и с максимальной точностью определить ее форму.
Паренхиматозная дистрофия печени
Паренхиматозная дистрофия печени имеет в основе развития связанного с ней патологического процесса изменения химико-физических и морфологических характеристик присущих клеточным белкам. Суть таких нарушений функционирования клеток представляет собой процесс гидратации, которому подвергается цитоплазма в результате того что в клетке имеет место коагуляция, денатурация, или же, напротив – явление колликвации. В тех случаях, в которых происходит нарушение белково-липидных связей, мембранные клеточные структуры характеризуются возникновением в них деструктивных процессов. Последствия таких изменений заключаются в развитии некротических процессов коагуляционного – сухого, или колликвационного – влажного характера.
Паренхиматозная дистрофия печени классифицируется по своим разновидностям как:
- Гиалиново-капельная
- Гидропическая
- Роговая дистрофия.
Острая печёночная дистрофия
Острая дистрофия печени (ОДП) чаще всего является осложнением гепатита А, который протекает в неблагоприятной форме. Отдельно патология развивается достаточно редко.
Заболевание мало исследовано, поэтому медики не могут с точностью ответить, как оно развивается. Также не понятно, существует ли связь с силой вируса или на патологический прогресс влияют какие-то другие факторы.

ОДП чаще всего является осложнением болезни Боткина
Отягченный паренхиматозный гепатит провоцируют следующие заболевания: бруцеллез, клещевая возвратная лихорадка, сифилис. Кроме того, повышается вероятность осложнений заболевания при беременности или после аборта. Эти факторы пагубно влияют на клетки печени, провоцируя тяжёлую дистрофию.
Симптомы ОДП на ранней стадии напоминают признаки гепатита А, поэтому существует риск значительного ухудшения состояния пациента. Патологический процесс поражает нервную систему, как следствие, нарушается мозговая деятельность. Заболевание проявляется бредом, беспокойством, судорогами, извержением рвотных масс. В таком случае больного нужно срочно госпитализировать в психиатрическое отделение.
Классификация
К паренхиматозным диспротеинозам относятся следующие патологические процессы:
- Гиали́ново-капельная дистрофи́я (внутриклеточный гиалино́з)
- Гидропи́ческая (вакуольная, водяночная) дистрофи́я
- Роговая дистрофи́я
- Первичные аминоацидопати́и
По современным представлениям только внутриклеточный гиалиноз и роговая дистрофия могут быть отнесены к паренхиматозным протеинопатиям, т.к. при этих процессах нарушается обмен белков (альбуминов и глобулинов крови, реабсорбируемых канальцевыми нефроэпителиоцитами при нефротическом синдроме; цитокератинов гепатоцитов при алкогольных поражениях печени; зрелого кератина). При первичных аминоацидопатиях происходит нарушение метаболизма прежде всего аминокислот. Зернистая и гидропическая дистрофии представляют собой морфологические варианты повреждения клетки, в процессе которого нарушается обмен всех веществ, а не только белков. Тем не менее, приведённая типология паренхиматозных диспротеинозов в отечественной патологической анатомии сложилась исторически и широко используется в практической работе патологоанатомов.
Белковая ДП
Белковая дистрофия печени (БДП) развивается вследствие расстройств метаболизма белков и возникает на фоне амилоидоза, гиалиновой или зернистой дистрофии.
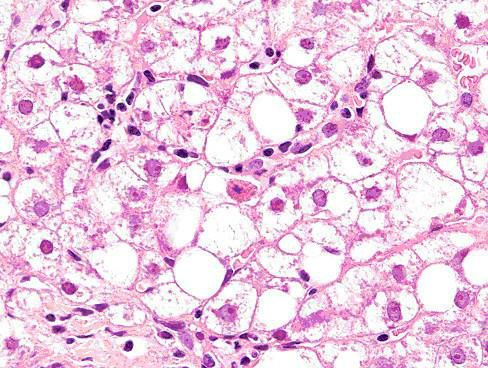
БДП проявляется вследствие нарушения обмена протеинов
При амилоидозе в тканях образовывается и откладывается амилоид (белково-полисахаридный комплекс).
Гиалиноз – это разновидность БДП, которым осложняется атеросклероз. Как правило, заболевание проявляется местно, например, в сосудистой стенке при формировании сгустка крови (тромб). Для патологии характерно образование полупрозрачных белковых структур, которые напоминают хрящ.
При БДП печень приобретает зернистую структуру, так как в протоплазме клеток возникают каплевидные и зерновидные образования. Они объединяются и заполняют внутриклеточное пространство. Белковые структуры уплотняются, нарушается работа клеток железы, как следствие, ткани печени отмирают.
НАРУШЕНИЯ ОБМЕНА НУКЛЕОПРОТЕИНОВ
Нуклеопротеины — вещества, состоящие из белка, соединенного либо с нуклеиновыми кислотами, либо с пуриновыми основаниями. Наибольшее значение в патологии нуклеопротеинов имеют дезоксирибонуклеиновая кислота (ДНК), рибонуклеиновая кислота (РНК) и пуриновые основания.
ДНК является основой хромосом и содержится в клеточном ядре, а РНК — переносчик генетической информации и располагается в ядрышках и цитоплазме клеток. При распаде нуклеопротеинов, помимо белка и ряда других соединений, образуются пуриновые основания, превращающиеся в мочевую кислоту, которая выделяется с мочой. При заболеваниях, сопровождающихся интенсивным распадом ядер клеток (гнойные воспалительные процессы, лейкозы и др.), возрастает содержание мочевой кислоты в крови — гиперурикемия и как следствие в моче — гиперурикурия. На содержание в организме и метаболизм мочевой кислоты оказывает влияние богатая пуринами пища — мясо, яйца, икра. При нарушениях обмена нуклеопротеинов может развиться ряд заболеваний, среди которых наибольшее значение имеет подагра.
Подагра.
В развитии заболевания определенную роль играет наследственная предрасположенность, а также употребление пищи, содержащей большое количество животных белков.
Патогенез. Болезнь заключается в повышенном образовании солей мочевой кислоты, что проявляется гиперурикемией и гиперурикурией. При этом периодически происходит выпадение кристаллов мочекислого натрия в синовиальных оболочках и хрящах мелких суставов, в основном пальцев рук и ног, но могут поражаться и голеностопные, и коленные суставы, сухожилия мышц, хрящи ушных раковин.
Морфология. Ткани в области выпадения кристаллов некротишруются, что сопровождается резкой болью. Вокруг очагов некроза и скоплений кристаллов мочекислых солей развивается продуктивное воспаление, завершающееся образованием рубцовой соединительной ткани. Повторяющиеся атаки подагры приводят к массивному развитию соединительной ткани и формированию так называемых подагрических шишек (tophi unci). При этом происходит деформация суставов. В почках кристаллы мочевой кислоты накапливаются в канальцах и собирательных трубках, в ответ на это развивается хроническое воспаление и атрофия почечной ткани — подагрические почки.
Внеклеточные диспротеинозы
К внеклеточным диспротеинозам относят патологический процесс, характеризующийся отложением между клетками соединительной ткани белковых веществ. К внеклеточным диспротеинозам относят гиалиноз и амилоидоз.
2.1. Амилоидоз
Амилоидная дистрофия характеризуется отложением в ткани гомогенного бесцветного плотного вещества, называемого амилоидом, то есть крахмалоподобным. Это название амилоид получил благодаря способности окрашиваться так же, как и крахмал, в синий цвет при обработке его йодом и серной кислотой, хотя он не имеет ничего общего с крахмалом.
По химической природе амилоид представляет собой белок (амилоидпротеид, близкий к глобулинам), находящийся в соединении с другими, недостаточно еще изученными химическими веществами. Установлено, что химический состав амилоида не всегда одинаков, чем объясняется неодинаковые его физические свойства.
Амилоидная дистрофия бывает общего и местного характера.
Общий амилоидоз проявляется отложением амилоидного вещества сразу во многих органах. Амилоид откладывается под аргирофильной мембраной мелких кровеносных сосудов, по ходу ретикулярных волокон и под базальной мембраной эпителиального покрова желез. При общем амилоидозе чаще поражается печень, селезенка, почки, надпочечники и др. органы.
Макрокартина.
При амилоидозе орган увеличивается в объеме, бледнее окрашен, плотной консистенции, у лошадей дряблой, поверхность разреза, особенно при сильной степени амилоидоза, восковидная, сухая.
Микрокартина.
В селезенке наблюдается отложение гомогенного бесструктурного вещества вокруг фолликулов селезенки и по ходу ретикулярных волокон; в печени между эндотелием капилляров и печеночными клетками; в почках под базальной мембраной эндотелия извитых канальцев или под аргирофильной мембраной эндотелия сосудистых клубочков и др. (рис.5).
Классификация
К паренхиматозным диспротеинозам относятся следующие патологические процессы:
- Гиали́ново-капельная дистрофи́я (внутриклеточный гиалино́з)
- Гидропи́ческая (вакуольная, водяночная) дистрофи́я
- Роговая дистрофи́я
- Первичные аминоацидопати́и
По современным представлениям только внутриклеточный гиалиноз и роговая дистрофия могут быть отнесены к паренхиматозным протеинопатиям, т.к. при этих процессах нарушается обмен белков (альбуминов и глобулинов крови, реабсорбируемых канальцевыми нефроэпителиоцитами при нефротическом синдроме; цитокератинов гепатоцитов при алкогольных поражениях печени; зрелого кератина). При первичных аминоацидопатиях происходит нарушение метаболизма прежде всего аминокислот. Зернистая и гидропическая дистрофии представляют собой морфологические варианты повреждения клетки, в процессе которого нарушается обмен всех веществ, а не только белков. Тем не менее, приведённая типология паренхиматозных диспротеинозов в отечественной патологической анатомии сложилась исторически и широко используется в практической работе патологоанатомов.
УГЛЕВОДНЫЕ СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
Углеводные стромально-сосудистые дистрофии связаны в основном с нарушением обмена глюкопротеинов и проявляются развитием в соединительной ткани, хрящах, в жировой клетчатке густой слизеподобной массы. Это так называемая слизистая дистрофии, обусловленная нарушениями функций эндокринных желез. Такая дистрофия развивается, например, при микседеме — заболевании, связанном с недостаточностью функции щитовидной железы. Ослизнение тканей может наблюдаться и при кахексии.
СМЕШАННЫЕ ДИСТРОФИИ
Смешанные дистрофии характеризуются нарушениями обмена веществ, которые проявляются одновременно в клетках и во внеклеточном матриксе. Смешанные дистрофии являются следствием нарушения обмена сложных белков и минералов.
Выделяют следующие сложные белки:
- хромопротеины — соединения, в которых белок связан с красящими веществами — пигментами;
- нуклеопротеины — комплекс белка и нуклеиновых кислот;
- липопротеины — соединения белка и липидов:
- глюкопротеины — соединения белка и углеводов.
Нарушения минерального обмена связаны с нарушениями метаболизма солей и их ионов.
Острая дистрофия печени
Острая дистрофия печени по преимуществу предстает в качестве осложнения, развивающегося на фоне неблагоприятного течения болезни Боткина. Случаи появления данного заболевания в автономной форме, как свидетельствует медицинская статистика, являются крайне редкими.
На сегодняшний день медицинские исследования в области изучения механизмов развития дистрофических явлений в печени не привели к получению однозначного ответа на вопрос о причине возникновения острой печеночной дистрофии. В настоящее время все еще до конца не изучены механизмы патологического прогресса этой тяжёлой болезни поражающей печень, и остается неясным существует ли корреляция с силой (вирулентностью) вируса, либо же имеет место воздействие каких-то иных факторов.
Привести к отягченному течению гепатитов паренхиматозного характера может наличие у пациента заболевания бруцеллёзом, возвратным тифом, сифилисом, а также состояние беременности и искусственное ее прерывание. Все это обуславливает высокую вероятность перерождения гепатитов в тяжелую форму дистрофии печени.
Острая дистрофия печени на начальной стадии воссоздает клиническую картину, схожую с началом развития болезни Боткина, что сопряжено со значительным ухудшением общего состояния больного. При этом поражению главным образом подвергается нервная система, что проявляется в появлении всевозможных расстройств мозговой деятельности. Пациенты начинают бредить, метаться по кровати, случаются судороги и рвота. В некоторых случаях появление таких состояний становилось обоснованием необходимости госпитализировать больного в психиатрическую клинику. С другой стороны, возможна иная, противоположная реакция ЦНС на развитие патологического процесса. Может появиться апатия и депрессивное состояние, существенное снижение жизненного тонуса организма, появиться повышенная сонливость. Вплоть до наступления бессознательного состояния и печеночной комы.
[], [], []
Диффузная дистрофия
Диффузно дистрофические изменения паренхимы печени – это весьма опасное состояние. Оно возникает в результате того, что гепатоциты не в состоянии нейтрализовать токсины, которые поступают в организм. Печёночные клетки не могут справиться с масштабным отравлением, как следствие, паренхиматозная ткань начинает отмирать, а на повреждённых участках разрастается фиброзная соединительная ткань. Диффузные изменения становятся всё более выраженными, а это грозит печёночной недостаточностью. Так проявляется диффузная ДП.
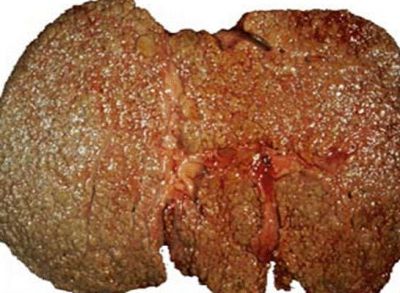
При диффузной трансформации паренхима печени отмирает
Дегенеративно дистрофические изменения печени чаще всего провоцирует аналогичный процесс в поджелудочной железе. Это обусловлено тем, что эти органы тесно связаны между собой.
Диета при дистрофии печени
Основные правила диеты:
- увеличить количество продуктов питания, богатых белком (кисломолочные продукты, мясо нежирных сортов);
- исключить углеводы (белый хлеб, сахар, рис, картошка);
- максимально снизить количество животных жиров (сливочное масло, жирная рыба и масло);
- обязательно включить в рацион не менее 2,5 л воды в сутки;
- исключить алкоголь;
- отказаться от жаренных, острых, соленых продуктов.
То, как будет проходить лечение дистрофии, напрямую зависит от человека. Если присутствует лишний вес, человек ведет малоподвижный образ жизни, следует полностью избавиться от таких факторов – заниматься спортом, но без особых физических нагрузок. О том, как лечить дистрофию физической гимнастикой можно узнать у врача.
Основными задачами диетического питания при дистрофии являются нормализация основных функций органа и возобновление холестеринового, жирового обмена; стимуляция выработки желчи.
Количество потребляемого жира в течение суток не должно превышать 50 г! Это очень важное условие. Кроме этого, необходимо исключить продукты, которые богаты холестерином
В этом случае можно будет не только помочь клеткам печени восстановиться, но и избежать тромбофлебита
Кроме этого, необходимо исключить продукты, которые богаты холестерином. В этом случае можно будет не только помочь клеткам печени восстановиться, но и избежать тромбофлебита.
Еще одно важное правило – блюда лучше готовить на пару или употреблять в вареном, запеченном виде. В этом случае они будут не только полезны для печени, но и сохранят все витамины
Что в обязательном порядке следует включить в рацион:
- супы на овощном бульоне с крупами, борщ;
- овощи;
- овощные салаты;
- неострый сыр, ветчина;
- вареное яйцо либо паровой омлет;
- овсянка, гречка, манная крупа;
- нежирные молочные продукты.
Что исключить:
- жирные продукты, грибные бульоны и грибы;
- морепродукты;
- репчатый лук в свежем виде, чеснок, томаты, редиска, бобовые;
- соленья и маринады;
- вяленые продукты;
- консервация;
- кофе, холодные или газированные напитки.
Очень важно не только лечить заболевание, но и принять все меры по его предупреждению. К методам профилактики относятся: здоровый образ жизни, контроль приема спиртных напитков, повышение иммунитета, забота о здоровье, занятия спортом
Только в этом случае можно будет предупредить такое заболевание, как жировая дистрофия печени. Следует запомнить, что если не лечить болезнь, она приведет к летальному исходу
К методам профилактики относятся: здоровый образ жизни, контроль приема спиртных напитков, повышение иммунитета, забота о здоровье, занятия спортом. Только в этом случае можно будет предупредить такое заболевание, как жировая дистрофия печени. Следует запомнить, что если не лечить болезнь, она приведет к летальному исходу.
https://youtube.com/watch?v=XotGAQ5Yc0o