Острый миелобластный лейкоз
Содержание:
- «Незаконное» проникновение в периферическую кровь
- Причины развития
- Острый миелобластный лейкоз: современное лечение больных
- Оценка состояния костного мозга
- Симптоматическая картина
- Симптомы и причины
- Клинические проявления заболевания
- Клиническая картина
- Происхождение
- Ðак леÑиÑÑ Ð»ÐµÐ¹ÐºÐ¾Ð·?
- ÐÑиÑÐ¸Ð½Ñ Ð¾ÑÑÑого миелоидного лейкоза
- Функция
- Лечение и прогноз
«Незаконное» проникновение в периферическую кровь
Однако бывают ситуации, когда клетки, которым надлежит еще «расти и развиваться» преждевременно покидают «родные пенаты». И если в норме о появлении бластных клеток в периферической крови не может быть и речи – они редкие «гости» в кровеносном русле, то при определенных патологических состояниях, вопреки природному запрету, и те, и другие все же выходят в кровеносное русло.
Бласты и миелобласты несколько повышены (до 2% по отношению к общей популяции лейкоцитов) при хронических формах лейкозов. А огромное количество бластов (бластемия) вообще указывает на серьезные изменения со стороны органов кроветворения и относится к значимым признакам острого лейкоза, форма которого будет впоследствии уточняться другими методами.
Особую обеспокоенность вызывает переход количества бластов 5% границы в крови больного, страдающего хроническим миелолейкозом – это может свидетельствовать о начале бластного криза и финальной стадии опухолевого процесса.

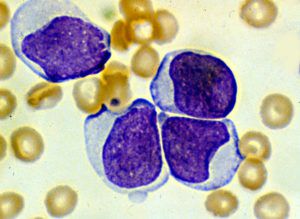
миелобласты в крови
Присутствие пропромиелоцитов, миелоцитов и наиболее приближенных к зрелым формам – метамиелоцитов, хоть и не является столь страшным показателем белой крови, однако все же указывают на серьезную патологию. Увеличение количества этих клеток до 5% чаще имеет причиной негематологическую патологию:
- Тяжело протекающее инфекционное заболевание любого происхождения: и бактериального (в основном), и вирусного;
- Развитие септического состояния;
- Различного рода интоксикации (бактериальная, алкогольная, солями тяжелых металлов);
- Опухолевый (злокачественный) процесс;
- Химио- и лучевая терапия;
- Прием отдельных лекарственных препаратов (анальгетики, иммуномодуляторы);
- Острые кровопотери;
- Кома, шок;
- Нарушение кислотно-щелочного равновесия;
- Чрезмерная физическая нагрузка.

присутствие миелоцитов и метамиелоцитов в крови
Между тем, значительный скачок миелоцитов, про- и мета- (до 10 – 25%), как правило, наблюдается в случае формирования миелопролиферативных заболеваний, которые и являются самыми основными причинами выхода из костного мозга созревающих форм и их свободного передвижения по кровеносным сосудам.
«Молодые да ранние»…
Под собирательным названием «миелопролиферативные опухоли» понимают хронические лейкозы, которые формируются на уровне самых молодых предшественников миелопоэза, все потомство которых – гранулоциты, моноциты, эритрокариоциты, мегакариоциты (кроме лимфоцитов), относится к опухолевому клону.

Хронический миелолейкоз, открывая список миелопролиферативных процессов, выступает в качестве типичного представителя опухолей, которые возникают из ранних (очень молодых) предшественников, миелопоэза дифференцирующихся до зрелого состояния.
Клеточный субстрат миелолейкоза берет начало от белого ростка кроветворения и представлен переходными (созревающими) формами гранулоцитов, в основном, нейтрофилов. Это говорит о том, что такие значимые клетки, как нейтрофилы, выполняющие столь важную роль в защите организма, страдают больше всех, поэтому понятно, почему это заболевание так плохо поддается лечению и, в конечном итоге, имеет летальный исход.
В начале болезни в крови отмечается сдвиг до миелоцитов и промиелоцитов, правда, численность их на первых порах еще незначительна. Помимо единичных промиелоцитов и несколько большего количества миелоцитов, в крови можно обнаружить представителей других клеточных популяций (эритрокариоциты, исчисляемые единицами, и высокий тромбоцитоз).
Развернутая стадия болезни дает значительное омоложение лейкоцитарной формулы и, при этом, кроме миелоцитов, в крови нередко повышены абсолютные значения и процентное содержание уже зрелых форм гранулоцитарного ряда: эозинофилов или базофилов (реже тех и других – «базофильно-эозинофильная ассоциация). Следует заметить, что резкое увеличение численности незрелых нейтрофилов является весьма и весьма неблагоприятным признаком, усложняющим течение болезни и прогноз.
Причины развития
Основной источник, из-за которого возникает миелоидный лейкоз — это мутация хромосом, ее еще именуют филадельфийской хромосомой. В процессе повреждения сегменты с хромосомами перестраиваются, что приводит к формированию молекулы ДНК с полностью обновленным строением. В дальнейшем клетки злокачественного характера копируются, и болезнь охватывает весь организм. Это является источником образования миелобластного лейкоза.
Заболевание может развиться под действием таких факторов:
- Облучение радиацией. Негативное влияние радиации на организм — неоспоримый факт. Подвергнуться облучению человек может из-за техногенной катастрофы или при работе на специфических участках производства. Но развитие лейкемии провоцирует проводимая прежде лучевая терапия при онкологии иного типа.
- Болезни вирусной природы.
- Электромагнитные облучения.
- Отдельные медикаменты. Это препараты от онкологических патологий, которые обладают активным токсическим влиянием на организм. Еще причиной развития миелоидного лейкоза могут стать некоторые химические субстанции.
- Генетическая склонность. Трансформации ДНК подвержены люди, унаследовавшие такую способность от собственных родителей.
При отсутствии своевременной и адекватной терапии заболевание может перейти в хронический миелолейкоз.
Важная информация: Как питаться (диета) при лейкозе крови и что можно кушать
Острый миелобластный лейкоз: современное лечение больных
Онкобольные после подтверждения диагноза, как правило, незамедлительно подвергаются химиотерапии. Целью такого лечения является перевод заболевания в стадию ремиссии. Цитостатические средства, в большинстве случаев, назначаются в комплексе с гормональными препаратами. Интенсивное медикаментозное лечение угнетает не только синтез атипичных клеток, но и образование физиологически нормальных элементов крови. В связи с этим у пациентов во время терапии ухудшается общее состояние, которое проявляется общей слабостью, приступами рвоты, спонтанными кровотечениями и недомоганием.
Позитивный результат химиотерапии, в основном, наступает через несколько недель. У многих пациентов наступает восстановление кроветворной функции. На этапе клинической ремиссии врачи-онкологи определяются с дальнейшей тактикой лечения. В онкологической практике пациентам с лейкозом можно провести операцию по трансплантации костного мозга или серию химиотерапевтических процедур.
Основное противораковое лечение, как правило, дополняется противовирусной и дезинтоксикационной терапиями.
Оценка состояния костного мозга
Очевидно, что слово «норма» может применяться только по отношению к костному мозгу, ибо миелоциты в крови априори присутствовать не могут. И повышены они там только в силу определенных причин, а не просто так. Поэтому далее – о месте миелоцитов в костном мозге.

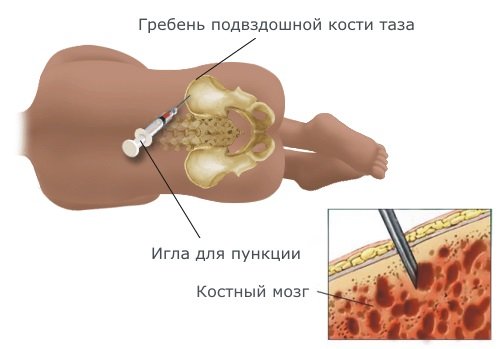
В настоящее время биопсия костного мозга и его исследование (цитологический анализ) является обязательной процедурой при подозрении на развитие гематологической патологии. Морфологические характеристики костного мозга после тестирования сопоставляют с показателями периферической крови.
Следует заметить, что при исследовании костного мозга (миелограмма) врачи обе генерации миелоцитов рассматривают вместе, не разделяя их на дочерние и материнские, поскольку подобное разделение не имеет абсолютно никакого значения ни для нормы, ни для патологии.
Таблица: клеточный состав костного мозга в норме (белый росток кроветворения)
| Элементы костного мозга | Границы нормальных значений,% | Средние значения,% |
|---|---|---|
| Ретикулярные клетки (клетки ретикулярной стромы) | 0,1 – 1,6 | 0,9 |
| Бласты | 0,1 – 1,1 | 0,6 |
| Миелобласты | 0,2 – 1,7 | 1,0 |
| Нейтрофилы: — промиелоциты — миелоциты — метамиелоциты — палочкоядерные — сегментоядерные | 1,0 – 4,1 7,0 – 12,2 8,0 – 15,0 12,8 – 23,7 13,1 – 24,1 | 2,5 9,6 11,5 18,2 18,6 |
| Все нейтрофильные элементы | 52,7 – 68, 9 | 60,8 |
| Индекс созревания нейтрофилов | 0,5 – 0,9 | — |
| Эозинофилы (все генерации) | 0,5 – 5,8 | 3,2 |
| Базофилы | 0 – 0,5 | 0,2 |
| Лимфоциты | 4,3 – 13,7 | 9,0 |
| Моноциты | 0,7 – 3,1 | 1,9 |
| Плазматические клетки | 0,1 – 1,8 | 0,9 |
Базофильные и эозинофильные миелобласты в здоровом костном мозге, как правило, не определяются (их трудно распознать), зато становятся довольно заметными при высокой эозинофильной реакции или хроническом миелолейкозе. Примерно то же самое происходит и с промиелоцитами – больше всех себя проявляют молодые клетки, которые стремятся стать нейтрофилами.
Что касается миелоцитов (эозинофильных, базофильных и нейтрофильных), то здесь ситуация несколько меняется, если к главному органу кроветворения нет претензий. Эозинофильный миелоцит, хотя ядром и похож на нейтрофильный, но отличается густой, заполняющей всю цитоплазму, зернистостью, базофильный миелоцит тоже легко распознается, он первым приобретает специфическую зернистость, которая негусто покрывает цитоплазму. При зарождении патологического процесса в костном мозге представители 3 генераций миелоцитов трудно различимы между собой и все напоминают нейтрофилы.
На стадии метамиелоцита, клетки уже «определились» в своей «профессии», поэтому специалисту, знающему их особенности и основные черты, нетрудно понять «кто есть кто». Между тем, описание ядра, цитоплазмы и других характеристик вряд ли заинтересует читателя, во всем этом трудно разобраться, тем более, если рядом нет микроскопа и клетку нельзя увидеть воочию. Поэтому не стоит попусту тратить время, более полезно будет рассказать о тех ситуациях, которые действительно могут волновать человека, например, о появлении миелоцитов у ребенка или их присутствии при беременности у женщины.
Симптоматическая картина
Клиника заболевания неспецифична на начальном этапе. Рак долго развивается в теле человека и проявляется под воздействием серьёзных факторов. Моноцитарный лейкоз обычно выявляется при диагностике других болезней.
При общих нарушениях развиваются анемия, кровоточивость и воспаления слизистой полости рта, инфекционные процессы, отмечается метастазирование, появляются симптомы интоксикации.
Когда угнетается красный росток костного мозга, больной испытывает:
- Вялость;
- Повышенную утомляемость;
- Головокружения;
- Тошноту;
- Нарушения зрения;
- Одышку;
- Сильное сердцебиение;
- Холод в конечностях;
- Цвет кожи становится бледно-серым.

При недостатке тромбоцитов развиваются:
- Частые кровотечения из носа;
- Подкожные кровоизлияния и синяки;
- Пролонгированные менструальные кровотечения;
- Спонтанные маточные или желудочно-кишечные кровотечения;
- Кровоточивость дёсен.
При поражении органов и систем человек испытывает боли в зависимости от локализации поражения:
- Для онкологического процесса в лёгких характерны кашель с кровью, одышка, боль в груди, признаки кислородного голодания. Развивается пневмония.
- Когда рак поражает головной мозг, у больного случаются приступы эпилепсии, провалы в памяти, расстройство зрения и нарушение речевых функций.
- Начинают возникать инфекционные и воспалительные процессы органов брюшной полости. Характерны боль в животе, спазмы, вздутие, расстройства стула. Развивается асцит. Из-за кровотечений кал становится черным, а рвота с небольшим количеством крови.
- Печень увеличивается и отекает. Выступает в правом подреберье. Нарушаются процессы вывода желчи. Развивается желтуха.
- Отекает и увеличивается селезёнка.
- При поражении скелета усиливается боль в костях и суставах в состоянии покоя.
По мере угнетения иммунитета симптомы приобретают более выраженный характер.
Симптомы и причины
Симптомы заболевания проявляются в первые пару месяцев. Это происходит потому, что поражённые лейкозом клетки начинают размножаться, подавляя функцию миелоидной ткани производить здоровые эритроциты, лейкоциты и тромбоциты. Специфических симптомов миелоидная лейкемия не имеет. Они напрямую зависят от того, в каких клетках происходят мутации, насколько сами лейкоциты дозревшие, и от множества других факторов.
Недостаток лейкоцитов приводит к снижению иммунитета. Больные становятся восприимчивыми к различным заболеваниям, простудным, например. Больные клетки, несмотря на то, что сами происходят от лейкоцитов, неспособны противостоять инфекциям, и функция защиты организма у них отсутствует. Симптомы дефицита лейкоцитов могут напоминать признаки гриппа или другого простудного заболевания.
Когда при миелоидном лейкозе снижено количество тромбоцитов, у больных отмечается плохая свёртываемость крови. Кожа таких пациентов легко повреждается, а кровотечения тяжело остановить. О роли тромбоцитов в организме мы писали выше. Могут наблюдаться кровотечения слизистых оболочек. На теле часто появляются синяки и кровоподтёки без сильного нажатия
Поражение эритроцитов (красных кровяных телец) проявляется анемией. Это бледность кожи, быстрая утомляемость (также один из основных симптомов для всех типов болезни) и отдышка.

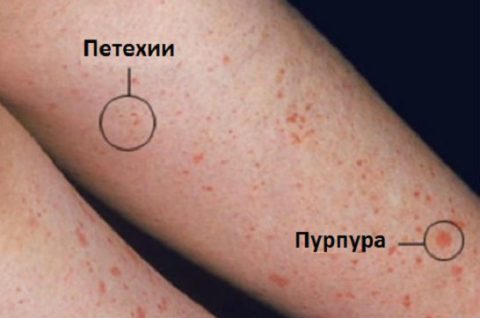
Общими симптомами могут быть потеря веса, повышенная температура, озноб. Петехии – крошечные пятнышки, которые проявляются на месте кровоизлияний, склонность к образованию гематом, даже при небольшом нажатии на кожу.
L o a d i n g . . .
Тест: А что вы знаете о человеческой крови?

ответ:
Когда на первых этапах больные клетки начинают накапливаться в костном мозге, то у пациентов наблюдаются сильные боли и ломота в руках и ногах. Людям больно ходить и совершать другую физическую активность.
Симптомы добавляются, когда раковые клетки начинают проникать в другие органы. Чаще всего это лимфатические узлы, печень, селезёнка, то есть те, которые непосредственно работают с кровью. Они нарушают их нормальную функцию, и поражённый орган начинает отекать. Абсолютно никакие органы не защищены от заболевания. Лейкозные клетки могут проникать также в головной мозг. Пациенты жалуются на головную боль, может возникнуть воспаление или паралич лицевого нерва.
Причины ОМЛ у детей и взрослых
Первопричины заболевания острым миелоидным лейкозом как у детей, так и у в взрослых плохо изучены. Но есть ряд способствующих факторов, при которых риск заболеть лейкозом возрастает.
Предлейкозные нарушения крови или миелодиспластический синдром характеризуются дефицитом в крови одной или нескольких клеток (тромбоцитов, эритроцитов и др.), дисплазией (изменением тканей) красного вещества. Делится на различные подтипы, в зависимости от вида недостающей клетки.
Высок риск заболеть, после различных видов химиотерапии, особенно в первые 5 лет после приёма препаратов.
Непосредственный контакт с различными химическими веществами, например, с бензолом (его роль в развитии лейкоза оспаривается) и другими растворителями, которые относят к группе канцерогенов.
Канцерогены – вещества различного воздействия, повышающие риски развития злокачественных опухолей. Подобные свойства могут иметь вещества различной природы: химические, излучение, ультрафиолет, бактерии или онкогенные вирусы. Медики подсчитали, что 80 – 90% всех онкозаболеваний возникали под действием таких факторов.
 Канцерогены в продуктах
Канцерогены в продуктах
Воздействие радиоактивного излучения – также повышает риск развития лейкоза. Доказано, что после ядерного удара в Хиросиме и Нагасаки и аварии на Чернобыльской АЕС количество заболеваний возросло из-за разрушения радиоактивным излучением белых кровяных телец.
Что касается генетической предрасположенности, например, у пациентов с синдромом Дауна риск заболеть миелобластным лейкозом выше в 10 раз
Наследственная предрасположенность не доказана. Есть сообщения о том, что заболеваемость среди родственников превышает среднестатистическую, но наследственность воспринимается как косвенный фактор заболевания.
Клинические проявления заболевания
При развитии ОМЛ наблюдают ряд синдромов:
- гиперпластический;
- геморрагический;
- анемический;
- интоксикацию и нейролейкоз;
- лейкостазы.
Они проявляются в виде типичной симптоматики, свидетельствующей о системном поражении всего организма. Для общей картины заболевания характерны постоянная усталость, плохой аппетит, бледность кожных покровов. Могут быть спонтанные скачки температуры, которые вначале принимают за проявления обычной простуды. В начале болезни увеличения лимфоузлов не наблюдают. Иногда возникают болезненные ощущения в ногах при ходьбе, которые поначалу проходят. Острый миелоидный лейкоз развивается постепенно, поэтому его симптомы появляются не сразу. Распознать заболевание в начальной стадии можно на основании развёрнутого анализа крови. Далеко не все пациенты подозревают у себя опасную болезнь, а тревожные симптомы часто списывают на усталость и переутомление.
На поздних стадиях ОМЛ возникают тяжёлая форма интоксикации, лейкостазы и нейролейкоз.
Гиперпластический синдром
Когда недозрелые клетки с током крови разносятся по организму, в органах человека возникает инфильтрация тканей. У больного появляются следующие признаки:
- увеличение периферических лимфоузлов, нёбных миндалин;
- увеличение селезёнки (спленомегалия);
- ощущение тяжести в области печени и её увеличение;
- отёчность верхних и нижних конечностей, лица;
- боли в мышцах, костях и суставах.
Отёки появляются вследствие разрастания средостенных лимфатических узлов. Увеличенные лимфоузлы сдавливают область верхней полой вены, и происходит нарушение кровообращения. Шея отекает, лицо приобретает синеватый оттенок, больному трудно дышать. В тяжёлых случаях возникает стоматит Венсана. Его симптомы: отёчность дёсен, боль, трудности при приёме пищи.
Геморрагический синдром
Незрелые миелобласты мешают выработке других кровяных клеток – в том числе и тромбоцитов. В результате этого возникает геморрагический синдром. Он выражается в типичных симптомах:
- истончение сосудистых стенок;
- кровотечения из носа и под кожей, образование множественных гематом на теле;
- кровь идёт долго, её трудно остановить;
- постоянно кровоточат дёсна.
Гематомы на теле появляются даже при незначительном надавливании на кожу. При геморрагическом синдроме высок риск кровоизлияния в мозг.

Анемический синдром
Для анемического синдрома характерны:
- сильная слабость;
- бледность кожных покровов;
- апатичное состояние;
- беспричинные головные боли;
- обмороки;
- головокружения;
- сердечные боли;
- желание есть мел.
Анемические проявления коварны тем, что их легче всего принять за обычное недомогание. Выпадение волос и ломкость ногтей больные часто принимают за недостаток витаминов. Если такое состояние не прекращается, нужно пройти обследование, чтобы заранее исключить злокачественную патологию крови.
Интоксикация и нейролейкоз
При интоксикации возникают:
- быстрая потеря веса;
- снижение аппетита;
- проливной пот;
- высокая температура (37-40С);
- тошнота и рвота;
- понос.
Вследствие снижения иммунитета на поздней стадии ОМЛ присоединяются бронхиты, воспаления лёгких и тяжёлые грибковые поражения слизистых.
Нейролейкозом называют комплекс симптомов, которые возникают при поражении мозга. Пациента мучают сильные головные боли, тошнота и рвота. Могут возникнуть приступы, похожие на эпилептические. При обследовании выявляют стойкое повышение внутричерепного давления. У больного ухудшается слух, нарушается речь, падает острота зрения. При системном поражении мозговых отделов возникают сумеречные состояния и нарушения восприятия окружающего мира.
Лейкостазы
Если при остром миелобластном лейкозе наблюдают общее замедление кровотока (или лейкостаз), прогноз жизни неутешителен. Число незрелых клеток в крови составляет 100 000 1/мкл и больше. Кровь становится густой и вязкой, происходит застой кровообращения во всех органах. Поскольку сосуды больного истончены, риск геморрагического инсульта становится во много раз выше. При лейкостазах высока частота летальных исходов.
Если лейкостаз возникает в малом кругу кровообращения, это чревато не только проблемами с дыханием, но и двусторонней пневмонией. Лечить её непросто, поскольку иммунная система больного подавлена, а содержание кислорода в крови падает с каждым днём. Все инфекционные заболевания, которые присоединяются на поздней стадии ОМЛ, протекают тяжело, с осложнениями, опасными для жизни.

Клиническая картина
Симптомы острого лейкоза взрослых и детей схожи между собой. На начальной стадии больной отмечает признаки простуды. Затем развиваются воспалительные процессы в ротовой полости (стоматит, гингивит), не поддающиеся лечению. При этой болезни возникают недомогание, утомляемость, боль в костях и суставах, обильное потоотделение, повышение температуры тела, тошнота, рвота с кровью. Больной отказывается от еды, быстро теряет вес. Кожные покровы приобретают серый бледный цвет. Обнаружить процесс может гемограмма, выполняемая для диагностики другого заболевания.
Нарушается процесс создания эритроцитов, развивается анемия. Больной жалуется на кровоточивость слизистых оболочек. Кожные покровы бледнеют, отмечается учащённое сердцебиение, больному тяжело двигаться из-за слабости в теле и головокружения, начинают выпадать волосы. Ухудшается состояние зубов и ногтей. Организм поражают грибки и бактерии.
Клиника заболевания развивается стремительно:
- Тело больного покрывается синяками и кровоподтеками. Часто возникают носовые и желудочные кровотечения. Воспаляются лимфатические узлы и миндалины. Происходит метастазирование в органы и позвоночник. Кожа покрывается инфильтратами. Лёгкие, сердце и почки перестают нормально функционировать.
- Поражается головной мозг. Развиваются эпилептические припадки, помутнение рассудка, нарушение зрения и речи. Продолжительность жизни резко сокращается.
Происхождение
Миелобласты происходят в конечном счёте от примитивных стволовых клеток ретикулума, так называемых гемангиобластов, находящихся между клетками стромы костного мозга. В процессе созревания и дифференцировки от гемангиобласта до миелобласта клетка проходит ещё несколько стадий: гемоцитобласт (плюрипотентная стволовая кроветворная клетка), CFU-GEMM (промиелобласт), CFU-GM (миеломонобласт). На каждой из стадий дифференцировки выбор возможных путей развития для клетки сужается. Так, на стадии гемангиобласта у клетки есть возможность стать либо кроветворной клеткой, либо клеткой эндотелия сосудов. На стадии гемоцитобласта этого выбора уже нет — клетка рекрутирована в кроветворный росток. Но сохраняется возможность дифференцировки по любому из путей дифференцировки кроветворных клеток — миелоидному или лимфоидному. На стадии CFU-GEMM возможность развития по лимфоидному пути уже закрыта, так как клетка уже избрала миелоидный путь дифференцировки, однако она всё ещё может выбрать разные пути дальнейшего развития — эритроидный, мегакариоцитарный или миеломоноцитарный. На стадии CFU-GM клетке остаётся возможность выбора уже только между моноцитарным и гранулоцитарным путём развития (эритроцитарный и тромбоцитарный пути развития для неё уже закрыты). И наконец, на стадии миелобласта клетка уже полностью унипотентная, избравшая гранулоцитарный путь развития. Процессы гранулопоэза и рекрутирования клеток-предшественников в ту или иную клеточную линию регулируются гуморальными агентами — цитокинами и хемокинами, такими, как колониестимулирующие факторы, интерлейкин 3.
Ðак леÑиÑÑ Ð»ÐµÐ¹ÐºÐ¾Ð·?
Ðейкоз â ÑеÑÑезное заболевание, коÑоÑое бÑÑÑÑо пÑогÑеÑÑиÑÑеÑ, еÑли не наÑаÑÑ ÑвоевÑеменное леÑение, Ñо ÑÑо пÑÐ¸Ð²ÐµÐ´ÐµÑ Ðº поÑледÑÑвиÑм.
СовÑÐµÐ¼ÐµÐ½Ð½Ð°Ñ Ð¼ÐµÐ´Ð¸Ñина пÑÐµÐ´Ð»Ð°Ð³Ð°ÐµÑ Ð»ÐµÑение оÑÑÑого лейкоза, коÑоÑÑй оÑнован на подÑоде в два ÑÑапа:
- ÐеÑвÑй ÑÑап назÑваеÑÑÑ Ñаза индÑкÑии. Ðлавной ÑелÑÑ, коÑоÑÑÑ Ð¿ÑеÑледÑÑÑ Ð²ÑаÑи на ÑÑом ÑÑапе ⤠Ñдаление непÑавилÑнÑÑ ÐºÐ»ÐµÑок из оÑганизма. ÐÑли не полное, Ñо болÑÑое колиÑеÑÑво. ÐлагодаÑÑ ÑÑÐ¾Ð¼Ñ Ð¼ÐµÑопÑиÑÑÐ¸Ñ Ð¼Ð¾Ð¶Ð½Ð¾ наÑаÑÑ ÑÑÐ°Ð´Ð¸Ñ ÑемиÑÑии.
- ÐÑоÑой ÑÑап назÑваеÑÑÑ Ð¿Ð¾ÑÑ-ÑемиÑÑиÑ. Ðогда наÑинаеÑÑÑ Ð²ÑоÑой ÑÑап леÑениÑ, оÑновной ÑелÑÑ Ð²ÑаÑей ÑвлÑеÑÑÑ Ð¿Ð¾Ð´Ð´ÐµÑжание ÑÑÑекÑа ÑеÑапии, ÑÑÑÑанение ÑÑÑекÑов болезни.
ÐÑоведение леÑÐµÐ½Ð¸Ñ Ð»ÐµÐ¹ÐºÐµÐ¼Ð¸Ð¸Â â ÑÑо Ñложное задание Ð´Ð»Ñ Ð²ÑаÑа, Ð±Ð¾Ð»ÐµÐ·Ð½Ñ ÑвлÑеÑÑÑ Ð½ÐµÐ¿ÑедÑказÑемой (как и вÑе ÑаковÑе заболеваниÑ), ÐºÐ°Ð¶Ð´Ð°Ñ Ñаза вклÑÑÐ°ÐµÑ ÑеÑапевÑиÑеÑкие меÑодÑ.
ÐÑиÑÐ¸Ð½Ñ Ð¾ÑÑÑого миелоидного лейкоза
Ð ÑакÑоÑам ÑиÑка, ÑпоÑобÑÑвÑÑÑÐ¸Ñ ÑазвиÑÐ¸Ñ ÑÑомоÑомнÑÑ Ð½Ð°ÑÑÑений, коÑоÑÑе и ÑÑиÑаÑÑÑÑ Ð½ÐµÐ¿Ð¾ÑÑедÑÑвенной пÑиÑиной ÑазвиÑÐ¸Ñ ÐÐÐ, пÑинÑÑо оÑноÑиÑÑ:
- неблагопÑиÑÑнÑÑ Ð½Ð°ÑледÑÑвенноÑÑÑ;
- ионизиÑÑÑÑее излÑÑение;
- конÑÐ°ÐºÑ Ñ Ð½ÐµÐºÐ¾ÑоÑÑми ÑокÑиÑеÑкими веÑеÑÑвами;
- пÑием ÑÑда лекаÑÑÑвеннÑÑ Ð¿ÑепаÑаÑов;
- кÑÑение;
- болезни кÑови.
Ð Ñоде иÑÑледований Ñакже бÑло вÑÑÑнено, ÑÑо пÑи ÑиндÑоме ÐлÑма, анемии Фанкони, ÑиндÑоме ÐаÑна веÑоÑÑноÑÑÑ Ð²Ð¾Ð·Ð½Ð¸ÐºÐ½Ð¾Ð²ÐµÐ½Ð¸Ñ Ð¾ÑÑÑого миелоидного лейкоза Ñакже ÑвелиÑиваеÑÑÑ.
ÐелÑÐ·Ñ Ð½Ðµ оÑмеÑиÑÑ Ð¸ наÑледÑÑвеннÑÑ Ð¿ÑедÑаÑположенноÑÑÑ Ð¿Ñи оÑÑÑÑÑÑвии генеÑиÑеÑÐºÐ¸Ñ Ð·Ð°Ð±Ð¾Ð»ÐµÐ²Ð°Ð½Ð¸Ð¹. ÐапÑимеÑ, еÑли Ñ Ð±Ð»Ð¸Ð¶Ð°Ð¹ÑÐ¸Ñ ÑодÑÑвенников бÑл диагноÑÑиÑован ÐÐÐ, Ñо ÑиÑк Ð²Ð¾Ð·Ð½Ð¸ÐºÐ½Ð¾Ð²ÐµÐ½Ð¸Ñ Ð±Ð¾Ð»ÐµÐ·Ð½Ð¸ повÑÑаеÑÑÑ Ð² 5 Ñаз. Ðаиболее ÑилÑно ÑÑÐ¾Ð¼Ñ Ð¿Ð¾Ð´Ð²ÐµÑÐ¶ÐµÐ½Ñ Ð¾Ð´Ð½Ð¾ÑйÑевÑе близнеÑÑ — ÑиÑк ÑоÑÑавлÑÐµÑ 25%.
Функция
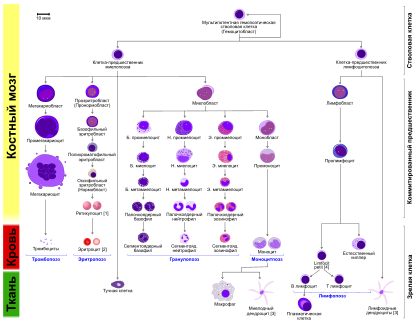
Диаграмма гемопоэза у человека
Гранулопоэз состоит из пяти последовательных стадий. Среди них миелобласт является первой клеткой, распознаваемой как принадлежащая к гранулоцитарному ростку костного мозга. Следующая стадия в процессе дифференцировки миелобласта — это промиелоцит, который, в свою очередь, может дать начало одному из трёх вариантов клеток-предшественников — нейтрофильному, базофильному или эозинофильному миелоциту. Тот, в свою очередь, превращается, соответственно, в нейтрофильный, базофильный или эозинофильный метамиелоцит («юный» гранулоцит). А нейтрофильный, базофильный или эозинофильный метамиелоцит превращается, соответственно, в нейтрофильный, базофильный или эозинофильный палочкоядерный гранулоцит. А тот, в свою очередь, в зрелый сегментоядерный (или «полиморфноядерный») нейтрофил, базофил или эозинофил. Весь этот процесс требует пяти последовательных делений клетки. Все эти пять делений происходят в течение трёх первых стадий гранулопоэза (миелобласт — промиелоцит — миелоцит). Далее идёт только созревание получившейся клетки-миелоцита, дальнейшего деления уже не происходит.
Лечение и прогноз
ОМЛ – возрастное заболевание. У детей оно встречается редко. Основной риск заболеть первичным лейкозом отмечается после 65 лет. Прогноз у молодых пациентов – лучше, так как они способны перенести максимально агрессивное лечение и более высокие дозы химиотерапии.
В целом при своевременном обращении к специалистам прогноз оптимистичный для большинства типов. Но определить это можно только после проведения анализов. Все подвиды миелоидного лейкоза индивидуально реагируют на лечение. В общих словах можно сказать, что терапия длится около 1,5 лет. Многое зависит от количества больных клеток и от того, насколько они проникли в другие органы. Также важный показатель – возраст больного. Но только правильно продиагностированный тип болезни и исследование самих хромосом позволят определить вероятность рецидива и продолжительность ремиссии.

2 этапа лечения ОМЛ
Непосредственно сама химиотерапия, её ещё называют индукция. Она проводится в условиях стационара. Препараты, которые используются при её проведении, называются цитостатическими. Например, «Цитарабин» – лекарство из группы антиметаболитов. Суть химиотерапии заключается в блокировании роста и деления клеток организма. Одновременно используется антрациклиновый антибиотик. Как правило, такая терапия проводится за 7 дней, и в первые три дня вводится дополнительно антибиотик. Это позволяет добиться ремиссии (снижение количества больных клеток) в 70 – 80% случаев. Когда пациент входит в состояние ремиссии, проводится консолидационное лечение.
После курса химиотерапии раковые клетки становятся незаметны при диагностике, но в организме они остаются, и в конце концов почти у всех больных возникает рецидив. Чтобы этого не произошло, проводят дополнительную терапию.
У разных типов миелоидного лейкоза – разный прогноз возникновения рецидива. Медики смотрят на морфологические и цитогенетические показатели изменённых хромосом. Так как отдельные виды более предрасположены к рецидиву, пациентам назначают более интенсивные курсы.
В отношении прогноза для пожилых людей отмечается, что у 30 – 40% после консолидационного лечения возникает рецидив. У молодых, до 65 лет, рецидив возникает в 10 – 15% случаев. Это чаще всего связано с тем, что молодые люди лучше переносят лечение
Важно понимать, что статистика берётся среди всех случаев во всех возрастах
Пересадка костного мозга и рецидив
Если после консолидационного лечения рецидив всё-таки произошёл, то назначают пересадку стволовых клеток костного мозга от живого донора. Чаще всего это родственник больного. При таком лечении есть риск, что его стволовые клетки будут отторгнуты. После этого проводятся курсы интенсивной химиотерапии. При необходимости, с целью профилактики нейролейкоза, может применяться облучение ЦНС.
Прогноз возникновения рецидивов после пересадки стволовых клеток повышается до 40%.
На исход лечения также влияет время между рецидивами, врачи говорят о неблагоприятных прогнозах, если время между ними составляет менее одного года.
В целом можно сказать, что острый миелобластный лейкоз – излечимое заболевание, вы обязательно справитесь, удачи.