Кардиопатия у детей и взрослых: причины, симптомы, лечение и возможные последствия
Содержание:
- Причины гипертрофической кардиомиопатии
- Методы лечения и прогноз длительности жизни
- Диагностика
- Наследственность как основная причина болезни
- Методы лечения гипертрофической кардиомиопатии
- Какие еще виды кардиомиопатии бывают?
- Что такое гипертрофическая кардиомиопатия
- Классификация ГКМП
- Лечение кардиомиопатии
- Симптомы и жалобы
- Диагностика кардиомиопатии
Причины гипертрофической кардиомиопатии
СН может развиться из-за того, что жёсткие и несинхронно сокращающиеся желудочки препятствуют диастолическому наполнению. Гипертрофия перегородки может также вызвать динамическую обструкцию выводного тракта ЛЖ (гипертрофическая обструктивная кардиомиопатия) или митральную регургитацию. Возникающие при нагрузке симптомы, аритмия и внезапная смерть — главные клинические проблемы.
Данное состояние — генетическое заболевание с аутосомно-доминантным типом передачи, высокой степенью пенетрантности, различной экспрессией. Существуют три типичные группы мутаций с разным фенотипом. Мутации тяжёлых цепей β-миозина ассоциируются с выраженной желудочковой гипертрофией. Мутации тропонина связаны с небольшой, иногда даже с отсутствующей гипертрофией, но выраженной перестройкой волокон миокарда, аномальным сосудистым ответом (например, индуцированная нагрузкой гипотония) и увеличенным риском внезапной смерти. Мутации в миозинсвязывающем белке С имеют тенденцию к позднему развитию и часто ассоциируются с гипертонией и аритмией.
Анализируя приведенное определение, следует остановиться на нескольких пунктах. Во-первых, для гипертрофической кардиомиопатии (ГКМП), в отличие от ДКМП, более четко определена роль наследственных факторов. Доля семейных случаев ГКМП составляет около 50%.
Установлены гены, кодирующие ряд белков саркомера (сократительных белков), мутации которых связаны с возникновением и развитием заболевания. На сегодня описано уже около 400 подобных мутаций в 11 генах.
К этим белкам относятся:
- β-тяжелые цепи миозина (30% белков миокарда, частота мутаций от общего числа мутаций — 30-50 %, на данный момент известно 80 мутаций);
- сердечный тропонин Т (5 % белков миофибрилл, частота мутаций — 10-15%, известных мутаций — более 20);
- α-тропомиозин (5 % белков миофибрилл, частота мутаций — менее 5%, известных мутаций — 8);
- Тропонин I;
- миозинсвязывающий белок С;
- мышечный I.IM-протеин, кодируемый СИРЗ-геном (открыт недавно; является регуляторным белком, осуществляющим дифференцировку кардиомиоцитов, а также взаимодействие белков цитоскелета).
Также в определении говорится о неравномерном характере гипертрофии, т.е. чаще в процесс вовлекаются отдельные сегменты миокарда, хотя возможно и равномерное поражение всего левого желудочка.
Гипертрофическая кардиомиопатия — генетически обусловленное аутосомно-доминантное заболевание. Однако существуют аллельные и неаллельные гетерогенные гены с множественными мутациями. В настоящее время выявлено 10 генов, ответственных за развитие данной патологии. Большинство из этих мутаций происходит в генах, ответственных за кодирование белков саркомеров (например, тяжелых цепей α-миозина, α-тропомиозина, тропонинов).
В отличие от дилатационной кардиомиопатии, такие мутации часто поражают белки саркомеров, участвующих в генерации сердечных сокращений, а не в их передаче. Тем не менее есть случаи, когда в одних и тех же генах наблюдают различные мутации, приводящие как к гипертрофической, так и к дилатационной кардиомиопатии (например, в гене α-актина). Обнаружены также мутации генов, кодирующих белки, не относимые к саркомерным.
Гистологически наблюдают нарушение взаиморасположения миофибрилл и выраженный фиброз. Мелкие внутристеночные артериолы также подвергаются гипертрофии. Изменения могут располагаться в виде чередующихся участков и преобладают в межжелудочковой перегородке. Подклапанная обструкция возникает между передней створкой митрального клапана и гипертрофированной перегородкой. Митральный клапан в систолу двигается в переднем направлении (сочетание разобщенной работы сосочковых мышц и высокой скорости потока в выносящем тракте желудочка). Происходит утолщение клапана и развитие митральной недостаточности.
Методы лечения и прогноз длительности жизни
Лечение гипертрофической кардиомиопатии включает медикаментозные и хирургические методы. Лекарства призваны поддержать состояние и убрать симптомы нарастающих осложнений. Полностью избавить человека от болезни может только пересадка сердца. Но существуют и другие оперативные вмешательства, облегчающие жизнь пациента:
- желудочковая септальная миоэктомия – эффективный и часто применяемый метод, который представляет собой удаление утолщенного участка межжелудочковой перегородки;
- септальная алкогольная абляция – обкалывание этиловым спиртом участков гипертрофированного миокарда, что приводит к их гибели и уменьшению толщины стенок левого желудочка;
- ресинхронизация – установка специальных электродов в сердце, которые подают соответствующие сигналы. Особенность состоит в том, что благодаря процедуре волна возбуждения идет с небольшой задержкой и захватывает сначала верхушку, затем перегородку органа, вследствие чего снижается давление в левом желудочке, и уменьшается степень обструкции его выходного отдела.
К хирургическому лечению гипертрофической кардиомиопатии есть строгие показания:
- высокое давление в выходном отделе ЛЖ в состоянии покоя (более 50 мм рт. ст.);
- выраженное утолщение стенки ЛЖ (больше 30 мм);
- яркая клиническая симптоматика (боли, обмороки).
Профилактика внезапной смерти и симптоматическая помощь
Для того чтобы облегчить симптомы гипертрофической кардиомиопатии, я назначаю следующие лекарственные препараты:
- бета-адреноблокаторы (Бисопролол, Метопролол) – эффективные медикаменты, уменьшающие выраженность клинических проявлений (одышки, болей в сердце, приступов сердцебиения) и замедляющие прогресс заболевания. Они снижают частоту сердечных сокращений и улучшают кровоснабжение миокарда. Однако всегда необходимо начинать их прием с малых доз. При замедлении ЧСС до 55 ударов в минуту и ниже нужно сразу же уменьшить количество потребляемого препарата;
- блокаторы кальциевых каналов (Верапамил, Дилтиазем) – их я назначаю, если у пациента есть противопоказания к приему бета-блокаторов (бронхиальная астма, хроническая бронхообструктивная болезнь легких, АВ-блокады II и III степени);
- калийсберегающие диуретики (Спиронолактон) – они используются при развитии хронической сердечной недостаточности для выведения лишней жидкости из организма;
- мочегонные (Торасемид, Гидрохлортиазид) я использую при тяжелых явлениях застоя крови: постоянной одышке, выраженных отеках ног, скоплении жидкости в грудной и брюшной полостях;
- антикоагулянты – у многих больных ГКМП довольно часто развивается фибрилляция предсердий, при которой повышен риск тромбообразования и инсульта, поэтому им необходим прием лекарственных средств, разжижающих кровь (Варфарин, Дабигатран, Ривароксабан);
- антиаритмические препараты – почти у всех пациентов с ГКМП возникают жизнеугрожающие нарушения ритма, с целью контроля которых могут быть назначены Дизопирамид, Амиодарон, Соталол.
Больным с ГКМП ни в коем случае нельзя применять вазодилататоры (лекарства, вызывающие расширение сосудов). К ним относятся нитраты, ингибиторы АФП, сартаны, а также блокаторы кальциевых каналов: Амлодипин и Нифедипин. Эти медикаменты вызывают рефлекторную тахикардию, т. е. в буквальном смысле «заставляют» сердце биться чаще, что только усугубляет заболевание, поэтому я стараюсь избегать их назначения.
Есть пациенты, у которых очень высок риск внезапной сердечной смерти – у них в семье уже были подобные случаи, они падают в обморок и имеют на ЭКГ тяжелые нарушения ритма (частые экстрасистолы, постоянные суправентрикулярные и желудочковые тахикардии и т. д.). Таким больным могут быть показаны:
- имплантация кардиовертера-дефибриллятора – вшивание под кожу грудной клетки специального устройства, способного сразу же купировать возникшее нарушение ритма. Оно позволяет свести риски смерти от аритмии практически к нулю;
- радиочастотная катетерная абляция – разрушение лазером участков патологической импульсации.
Диагностика
До появления клинической картины гипертрофическая кардиомиопатия может быть диагностирована случайно – при прохождении профилактического осмотра либо во время обследования по поводу какого-то другого кардиологического заболевания. Диагноз ставят, опираясь на данные анамнеза (истории) болезни и результатов дополнительных методов исследования. Жалобы больного являются информативными при прогрессировании патологии.
Из анамнеза необходимо выяснить, не диагностировалась ли такая же патология в семье.
Результаты физикального обследования будут следующими:
- при осмотре – отмечается бледность с синюшным оттенком кожных покровов и видимых слизистых оболочек;
- при пальпации (прощупывании) – при изучении верхушечного толчка отмечается его смещение;
- при аускультации сердца (прослушивании фонендоскопом) – выявляется систолический шум, может быть обнаружено усиление тонов сердца из-за необходимости желудочка сокращаться сильнее, чтобы обеспечить выталкивание крови в сосудистую систему. При наличии аритмий их можно обнаружить аускультативно.
Также в ряде случаев отмечаются нарушения со стороны центральной гемодинамики (тока крови):
- аритмичный пульс;
- повышение артериального давления.
Из инструментальных методов исследования в диагностике описываемого заболевания информативными являются следующие:
- обзорная рентгенография органов грудной клетки – она позволяет обнаружить изменение контуров сердца (а именно за счет увеличения пораженного желудочка) и сопутствующие нарушения со стороны крупных сосудов. Но метод является информативным при прогрессировании описываемой патологии – это не удовлетворяет клиницистов, так как болезнь при этом может уже достигнуть критической точки развития;
- рентгенография сердца с контрастированием пищевода – пациент принимает внутрь порцию контрастного вещества, затем проводят рентгенографическое исследование сердца, с помощью полученных снимков оценивают размеры и другие характеристики желудочков;
- электрокардиография (ЭКГ) – графическое записывание биопотенциалов сердца. Электрокардиография не является специфическим методом выявления гипертрофической кардиомиопатии, но она позволяет определить нарушения ритма, которые могут возникать при описываемом заболевании, а также оценить работу сердца на фоне разрастания миокарда;
- чреспищеводная электрокардиография – благодаря близости расположения электродов к миокарду результаты ЭКГ будут более точными;
- холтеровское исследование – пациенту устанавливают специальный аппарат, который фиксирует на протяжении 24 часов ритм сердца. Метод позволяет выявить те нарушения электрической активности сердца, которые не получилось обнаружить при проведении обычной ЭКГ;
- эхокардиография (ЭхоКГ) – выявление изменений структуры миокарда с помощью ультразвуковых волн;
- вентрикулография – в желудочки сердца вводят контрастное вещество, затем делают рентгенологические снимки, по ним оценивают строение стенки желудочков, состояние их полостей, а также функциональную активность;
- аортография – во время проведения данного метода в аорту вводят контрастное вещество, после чего делают рентгеновские снимки, по которым определяют нарушения аорты, возникшие вследствие нарушений работы левого желудочка на фоне описываемой патологии;
- магнитно-резонансная томография (МРТ) – высокая диагностическая способность метода (благодаря послойному изучению структур) позволяет выявить тканевые нарушения миокарда;
- биопсия миокарда – забор фрагментов тканей сердечной мышцы с последующим изучением под микроскопом.
Лабораторные методы исследования менее информативны в диагностике описываемого заболевания и, как правило, проводятся для оценки его последствий. Это:
- общий анализ крови – повышение количества лейкоцитов (лейкоцитоз) и СОЭ может сигнализировать про воспалительное поражение внутренней оболочки сердца, которое способно развиться на фоне данной болезни;
- анализ газового состава крови – по содержанию кислорода и углекислого газа можно косвенно судить про степень нарушения кровообращения;
- коагулограмма – позволяет оценить состояние свертывающей системы крови и риск тромбообразования, которые существуют при этой патологии;
- гистологическое исследование – под микроскопом изучают тканевое строение биоптата. При этом в нем нередко отмечается замещение мышечных структур на соединительнотканные;
- цитологическое исследование – под микроскопом изучают клеточное строение биоптата. Клетки в образце тканей расположены хаотично.
Наследственность как основная причина болезни
По наследству передаются генные мутации, которые нарушают синтез сократительных белков сердца. Вследствие этого явления провоцируетсяпатологический рост некоторых волокон сердечной мышцы.
Установлено, что при гипертрофической кардиомиопатии уплотнение левого желудочка никак не связано с пороками сердечной мышцы, гипертонией, ишемической болезнью сердца и другими недугами, при которых могут возникать похожие изменения.
Вторая половина случаев патологии обусловлена такими причинами:
- Спонтанная мутация генов, не связанная с наследственным фактором. При этом наблюдаются спонтанные и стойкие изменения генов, которые регулируют синтез сократительных белков. В свою очередь, эти мутации могут вызываться курением, вредными условиями трудами (радиационные излучения), некоторыми инфекциями, а также во время беременности.
- Длительная стойкая гипертония может спровоцировать вторичную гипертрофическую кардиомиопатию. Развивается она у людей преклонного возраста с патологическими изменениями структуры сердца, которые произошли еще при их развитии в утробе матери.
- Возраст от 20 до 40 лет. В этом случае риск возникновение патологии увеличивается при наследственной предрасположенности.
Вредные воздействия на организм беременной женщины – пагубные привычки, инфекционные заболевание, ионизирующие излучения.
Состояние здоровья многих больных может стабилизироваться и улучшаться при естественном течении болезни.
Гипертрофическая кардиомиопатия у детей может диагностироваться в любом возрасте. Симптомы патологии у ребенка схожи с клиникой взрослого. У детей и молодых людей риск осложнений гораздо увеличивается, если их родители или члены семьи также страдают от этой патологии.

Симптоматика появляется без предшествующих воспалительных явлений, провоцирующих факторов. Причина – генетический дефект, имеющий наследственный, семейный характер.
- В результате мутации генов нарушается синтез сократительных белков миокарда.
- Мышечные волокна имеют неправильное строение, расположение, местами заменяются соединительной тканью.
- Изменённые кардиомиоциты сокращаются не координировано, нагрузка на них возрастает, волокна утолщаются, гипертрофируется вся толща миокарда.
Как показывает статистика, гипертрофическая кардиомиопатия развивается примерно у 1% людей. Преимущественно болеют мужчины 30-50 лет.
Примерно у 20% больных развивается коронарный атеросклероз, а у 10% пациентов состояние осложняется инфекционным эндокардитом. Иногда, редко, встречается гипертрофическая кардиомиопатия и у детей.
Гипертрофическая кардиомиопатия (схема)
Гипертрофическая кардиомиопатия чаще всего носит наследуемый характер. Основу её составляет передающиеся по наследству дефектные гены, кодирующие синтез сократительного белка миокарда. Гены могут мутировать спонтанно из-за внешних факторов.
Поскольку врачи до конца не определились с первичными и вторичными формами гипертрофической кардиомиопатии, некоторые из докторов утверждают, что к появлению кардиомиопатии может привести долгое и стабильное повышение АД у пациентов старшего возраста, если во время их внутриутробного развития произошли изменения структур сердца.
Симптомы гипертрофической кардиомиопатии во многом зависит от её формы. Так, необструктивная практически не доставляет пациенту дискомфорта, поскольку не нарушает кровоток. Состояние сопровождается одышкой, нарушениями тока крови из желудочка или неритмичный пульс, и то при выполнении физических нагрузок.
Обструктивная гипертрофическая кардиомиопатия выражается:
- одышкой;
- головокружениями;
- обморочными состояниями;
- артериальной гипотензией;
- экстрасистолией;
- пароксизмальной тахикардией;
- сердечной астмой;
- отёками лёгких;
Примерно в 70% случаев у пациентов наблюдаются приступы ангинозных болей.
Причиной для внезапной сердечной смерти, развивающейся на фоне гипертрофической кардиомиопатии, становятся нарушения сердечного ритма, а также:
- фибрилляция желудочков;
- атриовентрикулярная блокада;
- острый инфаркт миокарда;
Состояние развивается стремительно, и уже в течение часа после первых симптомов наступает летальный исход.
Методы лечения гипертрофической кардиомиопатии
Терапевтические мероприятия позволяют только добиться временной стабилизации состояния больного и имеют симптоматический характер.
Основными целями лечения в данном случае являются:
- улучшение диастолической функции левого желудочка;
- купирование нарушений ритма;
- снижение градиента давления;
- купирование ангиозных приступов.

Консервативная терапия
Медикаментозное лечение патологии предусматривает применение следующих лекарственных средств:
- Бета-адреноблокаторы. Препараты этой фармакологической группы стабилизируют ритм сердца, снижают сократимость миокарда, нормализуют тонус сосудов. Бета-адреноблокаторы расслабляют сердечную мышцу в то время, пока левый желудочек наполняется кровью. Современными препаратами данной группы, которые обычно назначают при рассматриваемой патологии, являются Целипрес, Обзидан, Карведилол, Эналаприл-Фармак, Амиодарон.
- Антиаритмические препараты. Обычно применяют Дизопирамид. Препарат снижает градиент давления и устраняет симптомы патологии: одышку, боль за грудиной. Также этот медикамент повышает толерантность к физическим нагрузкам.
- Антагонисты кальция. Препараты данной группы снижают концентрацию кальция в системных коронарных артериях. С их помощью удается достичь улучшения диастолического расслабления левого желудочка, снижения сократимости миокарда. Антагонисты кальция также оказывают выраженное антиаритмическое и антиангинальное действие. Для лечения патологии рекомендуют Финоптин,Кардил, Амиодарон.
- Диуретики (Лазикс, Фуросемид). Их назначают при развитии застойной сердечной недостаточности.
При гипертрофической кардиомиопатии противопоказан прием лекарственных средств, принадлежащих к группам сердечных гликозидов, нитритов, нифедипина. Это ограничение связано с тем, что данные медикаменты способствуют усилению обструкции.
Оперативное вмешательство
Кроме приема лекарственных препаратов, при лечении пациентов с гипертрофической кардиомиопатией могут прибегать к хирургическим методам. Это единственный способ сохранения жизни пациента с тяжелой формой патологии.
Оперативное вмешательство предполагает удаление гипертрофированной мышечной ткани в межпредсердной перегородке.
К основным методам хирургического лечения в данном случае относятся:
- Миотомия – удаление внутренней области межжелудочковой перегородки.
- Этаноловая абляция. Метод заключается в осуществлении прокола в перегородке, куда затем вводится концентрированный раствор медицинского спирта. Количество вводимого вещества – от 1 до 4 мг. Подобная манипуляция становится причиной инфаркта у пациента. Таким образом происходит истончение перегородки. Мероприятие проводится под контролем УЗИ.
- Вживление трехкамерного электростимулятора. Прибор стимулирует внутрисердечное кровообращение и предотвращает развитие осложнений.
- Имплантация кардиовертера-дефибриллятора. Суть процедуры состоит в том, что в мышцу живота или грудной клетки имплантируют прибор, соединенный с сердцем при помощи электродов. Это позволяет фиксировать ритм сердца и в случае сбоя восстанавливать его.
Выбор методики осуществляется в индивидуальном порядке.
Коррекция образа жизни
Пациентам с гипертрофической кардиомиопатией показано ограничение физических нагрузок и соблюдение низкосолевой диеты.
Какие еще виды кардиомиопатии бывают?
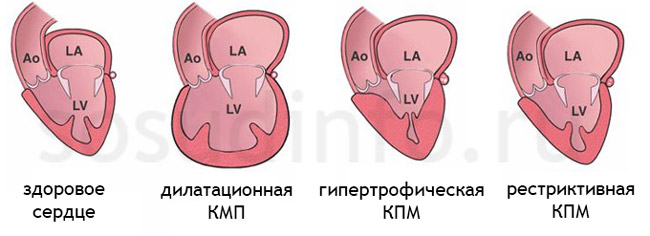
Кроме гипертрофической, существуют дилатационный и рестриктивный типы КМП.
- В первом случае сердечная мышца утолщается, а сердце в целом увеличивается в размерах.
- Во втором случае сердце также увеличивается, но не за счет утолщенной стенки, а за счет перерастяжения истонченной сердечной мышцы увеличенным объемом крови в полостях, то есть сердце напоминает “мешок с водой”.
- В третьем случае нарушается нормальное расслабление сердца не только за счет ограничений со стороны перикарда (спайки, перикардит и т. д.), но и за счет выраженных диффузных изменений в структуре самого миокарда (эндомиокардиального фиброза, поражения сердца при амилоидозе, при аутоиммунных заболеваниях и др).
Что такое гипертрофическая кардиомиопатия
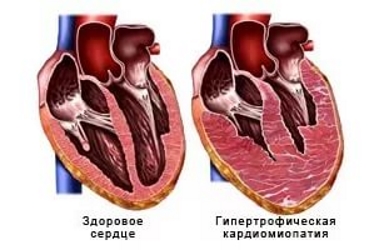
Гипертрофическая кардиомиопатия — это весьма редкое наследственное, т.е. первичное по происхождению заболевание, характеризующееся гипертрофией левого желудочка при отсутствии каких-либо признаков врожденных и приобретенных пороков сердца, системной артериальной гипертензии и других форм патологии, способных вызывать его гипертрофию.
Расстройство имеет переменную картину и имеет высокую частоту внезапной смерти. На самом деле, гипертрофическая кардиомиопатия (ГКМ) является основной причиной внезапной сердечной смерти у детей до и подросткового возраста. Отличительной чертой этого расстройства является гипертрофия миокарда, которая часто асимметрична и возникает при отсутствии явного стимула гипертрофии. Эта гипертрофия может возникать в любой области левого желудочка, но часто включает межжелудочковую перегородку, что приводит к обструкции потока через левый желудочек тракта оттока.
У многих больных, особенно детей, с ГКМ может не иметься симптомов. Тщательная оценка шумов в сердце может выявить заболевание.
Гипертрофическую кардиомиопатию классифицируют по ее анатомическому паттерну, наблюдаемому в левом желудочке. Наиболее часто (примерно в 90% случаев) гипертрофия является асимметричной и относится к желудочковой перегородке. При гистологическом исследовании в ней обнаруживают беспорядочно расположенные кардиомиоциты, образующие хаотическую, а не обычную упорядоченную, характерную для нормального миокарда структурированную ткань с параллельно расположенными миоцитами. При этом в некоторых гипертрофированных кардиомиоцитах выявляют дистрофические изменения, вплоть до необратимой альтерации с развитием заместительного склероза. Кроме того, постоянным патогистологическим признаком гипертрофической кардиомиопатии является увеличение содержания в миокарде соединительной ткани вследствие интерстициального фиброза и в меньшей степени заместительного склероза.
Функционально гипертрофическую кардиомиопатию чаще всего классифицируют по механизму обструкции пути оттока крови из левого желудочка.
Примерно у четверти больных гипертрофической кардиомиопатией гипертрофия перегородки является причиной обструкции пути оттока крови из левого желудочка во время систолы.
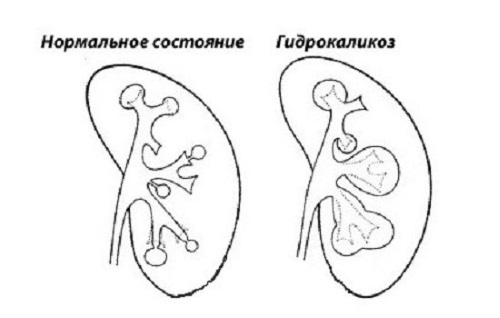
Во время диастолы желудочек заполняется через открытое митральное отверстие. При этом из-за утолщения (гипертрофии) и фиброзирования стенки желудочка процесс его заполнения (обозначен волнистой стрелкой) затрудняется. В ранний период систолы (период выброса начальной порции крови из левого желудочка) поток крови проходит через открытый аортальный клапан аномально близко (опять же из-за утолщенной стенки) к митральному отверстию.
В середине систолы утолщенная перегородка, суживающая выходной путь кровотоку, детерминирует эффект Вентури (ГУ): перетягивание передней створки митрального клапана к перегородке (митральная створка может даже к ней прикоснуться), что вызывает динамическую обструкцию аортального отверстия. При этом сердечный выброс существенно уменьшается, несмотря на значительное увеличение внутрижелудочкового давления. Описанное препятствие выбросу крови является патогенетически значимым преимущественно в середине или конце систолы, т.е. в моменты наибольшей постнагрузки на желудочек.
В условиях, когда гипертрофированное сердце подвергается внезапному увеличению постнагрузки, кривая диастолического давления смещается вверх и принимает более крутой угол подъема, а кривая иэоволюмического систолического давления перемещается лишь немного вверх по сравнению с аналогичной кривой в норме.
При этом ударный объем уменьшается, несмотря на заметное повышение конечного диастолического давления. Патогенетической основой всех этих изменений является уменьшение комплаенса и растяжимости гипертрофированного сердца.
Классификация ГКМП
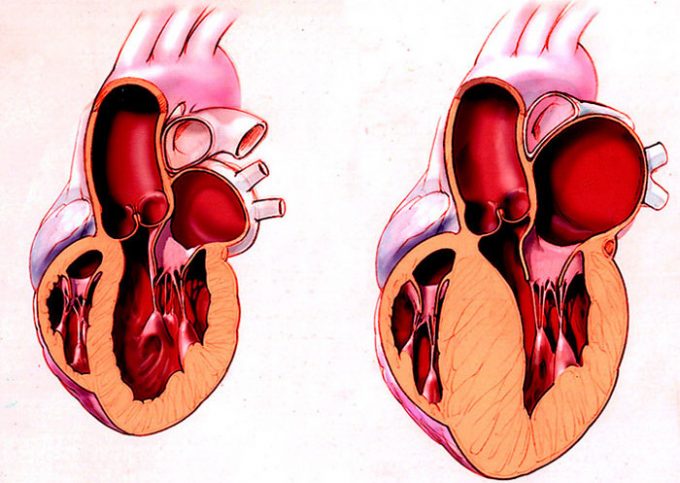
Обструктивная гипертрофическая кардиомиопатия
Для гипертрофической кардиомиопатии предложена гемодинамическая классификация, в рамках которой выделяют следующие ее формы:
- Обструктивная форма. Само слово «обструкция» обозначает какое-то препятствие. При обструктивной форме гипертрофической кардиомиопатии создается определенное препятствие для прохождения крови из левого желудочка (реже правого желудочка) в выносящие сосуды. Это происходит по причине неравномерной гипертрофии межжелудочковой перегородки. Утолщение перегородки вследствие ее гипертрофии может быть в верхней, средней или апикальной (верхушечной) части. Кроме асимметричной гипертрофии может иметь место и симметричная. Обструктивная форма подразделяется на 4 стадии в зависимости от градиента давления в левом желудочке (разница давления выше и ниже места сужения просвета).
- Необструктивная форма. К такой форме относится равномерная гипертрофия миокарда желудочка, которая носит название концентрической. В эту же группу относят формы неравномерной гипертрофии межжелудочковой перегородки, когда нет препятствия изгнанию крови из желудочка.
- Латентная форма. Занимает промежуточное положение между указанными двумя.
Течение заболевания может иметь несколько вариантов:
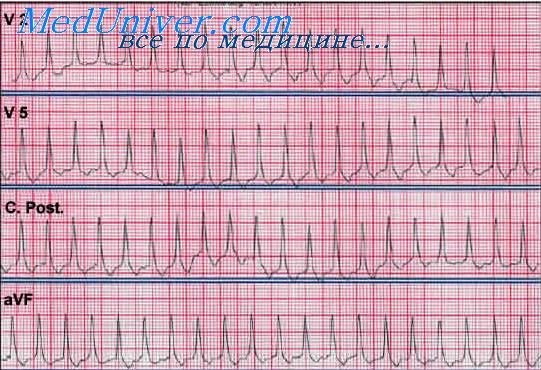
Нарушений сердечного ритма при гипертрофической кардиомиопатии
- Доброкачественное, стабильное течение. Нет прогрессирования заболевания.
- Внезапная смерть. В некоторых случаях причиной смерти до этого момента «здорового» человека является гипертрофическая кардиомиопатия.
- Прогрессирующее течение. Симптомы сердечной недостаточности усиливаются, снижается переносимость физической нагрузки (ФН), появляются симптомы в покое.
- Возникновение нарушений сердечного ритма. Частым проявлением гипертрофической кардиомиопатии является мерцательная аритмия. Ее наличие создает условия для образования тромбов в полости предсердий и желудочков, которые могут, отрываясь, уноситься с током крови и перекрывать просвет сосудов.
- «Конечная стадия» характеризуется изменением структуры левого желудочка и снижение его сократительной функции.
Лечение кардиомиопатии
например, прием противовоспалительных средств и антибиотиков при инфекционных поражениях миокардас периодическим посещение врача-кардиолога или терапевтаЛечение кардиомиопатии может вестись следующими способами:
- медикаментозное лечение;
- хирургическое лечение;
- профилактика осложнений.
Медикаментозное лечение
Препараты, используемые в лечении кардиомиопатий различных видов
| Группа препаратов | Механизм действия | Наименование препарата | Рекомендуемая дозировка |
| Ингибиторы ангиотензинпревращающего фермента | Препараты данной группы снижают артериальное давление и нагрузку на сердце. Это замедляет прогрессирование сердечной недостаточности. | Эналаприл | От 2,5 мг 2 раза в сутки. |
| Рамиприл | От 1,25 мг 1 раз в сутки. | ||
| Периндоприл | От 2 мг 1 раз в сутки. | ||
| Бета-адреноблокаторы | Даная группа препаратов хорошо борется с аритмиями и тахикардией, которые наблюдаются у большинства больных с кардиомиопатиями. | Метопролол | 50 – 100 мг 2 раза в сутки. |
| Пропранолол | 40 – 160 мг 2 – 3 раза в сутки. | ||
| Блокаторы кальциевых каналов | Также борются с аритмией и стабилизируют работу сердечной мышцы. | Верапамил | 40 – 160 мг 3 раза в сутки. |
| Дилтиазем | 90 мг 3 – 4 раза в стуки. |
мочегонные препараты
Профилактика осложнений
особенно при первичных кардиомиопатияхПрофилактика осложнений кардиомиопатии предполагает соблюдение следующих правил:
- Умеренная физическая нагрузка. Полный отказ от занятий спортом – не лучший выход, так как движения способствуют циркуляции крови и облегчают работу сердца. Однако тяжелые физические нагрузки резко увеличивают потребность миокарда в кислороде и повышают риск ишемии.
- Соблюдение диеты. Диета при кардиомиопатиях не отличается от таковой при сердечной недостаточности. Следует ограничить употребление животных жиров (они способствуют развитию атеросклероза), соли (до 3 – 5 г в сутки, для борьбы с отеками), алкоголя. Переход на здоровое питание (кисломолочные продукты, овощи и фрукты) улучшит самочувствие пациента в целом и облегчит его состояние. Иногда рекомендуется консультация диетолога для составления индивидуального меню с поступлением оптимального количества питательных веществ.
- Отказ от курения. Курение ведет к развитию атеросклероза и воздействует на нервную систему, регулирующую работу сердца. При кардиомиопатиях это может спровоцировать ишемию или приступ аритмии.
- Регулярное обследование у кардиолога. Кардиомиопатии обычно прогрессируют со временем. В связи с этим необходимо следить за состоянием здоровья и периодически проходить определенные диагностические процедуры (ЭКГ, ЭхоКГ). Это позволит вовремя внести изменения в курс лечения и предотвратить осложнения болезни.
Симптомы и жалобы
Сердечная недостаточность
В основе одышки в покое и при физической нагрузке, ночных приступов сердечной астмы и утомляемости лежат два процесса: повышение диастолического давления в левом желудочке из-за диастолической дисфункции и динамическая обструкция выносящего тракта левого желудочка. Повышение ЧСС, снижение преднагрузки, укорочение диастолы, усиление обструкции выносящего тракта левого желудочка (например, при физической нагрузке или тахикардии) и снижение податливости левого желудочка (например, при ишемии) усугубляют жалобы. У 5—10% больных с гипертрофической кардиомиопатией развивается тяжелая систолическая дисфункция левого желудочка, происходит дилатация и истончение его стенок
Ишемия миокарда
Ишемия миокарда при гипертрофической кардиомиопатии может возникать независимо от обструкции выносящего тракта правого желудочка. Ишемия миокарда клинически и электрокардиографически проявляется так же, как обычно. Ее наличие подтверждается данными сцинтиграфии миокарда с 201Тl, позитронно-эмиссионной томографии, повышением продукции лактата в миокарде при частой стимуляции предсердий. Точные причины ишемии миокарда неизвестны, однако в основе ее лежит несоответствие между потребностью в кислороде и его доставкой. Этому способствуют следующие факторы.
Поражение мелких коронарных артерий с нарушением их способности расширяться.
Повышение напряжения в стенке миокарда, возникающее из-за замедленного расслабления в диастолу и обструкции выносящего тракта левого желудочка.
Снижение числа капилляров по отношению к числу кардиомиоцитов.
Снижение коронарного перфузионного давления.
Обмороки и предобморочные состояния
Обмороки и предобморочные состояния возникают из-за снижения мозгового кровотока при падении сердечного выброса. Они обычно случаются при физической нагрузке или аритмиях.
Внезапная смерть
Годичная смертность при гипертрофической кардиомиопатии составляет 1—6%. Большинство больных умирает внезапно.Риск внезапной смерти у разных больных разный. У 22% больных внезапная смерть — первое проявление болезни. Внезапная смерть чаще всего бываету детей старшего возраста и молодых; до 10 лет она встречается редко. Примерно 60% внезапных смертей возникают в покое, остальные — после тяжелой физической нагрузки. Нарушения ритма и ишемия миокарда могут запускать порочный круг артериальной гипотонии, укорочения времени диастолического наполнения и усиления обструкции выносяшего тракта левого желудочка, что в конце концов приводит к смерти.
Диагностика кардиомиопатии
Диагностику КМП следует доверять только опытному специалисту, поскольку клиническая картина при различной патологии имеет схожие признаки.
Сначала врач собирает анамнез и осматривает пациента (обращает внимание на цвет кожи, уточняет наличие отеков, измеряет ЧСС и АД, выслушивает сердце и легкие стетоскопом). Далее назначаются лабораторные и инструментальные исследования:
Далее назначаются лабораторные и инструментальные исследования:
- анализы крови (клинический, биохимический, гормональный статус, липидограмма и т.д.);
- электрокардиография (ЭКГ);
- холтер-мониторинг ЭКГ;
- эхокардиография (УЗИ сердца);
- рентгенография;
- коронарография;
- МРТ, КТ сердца.